TERAPÉUTICA FARMACOLÓGICA DE LA HEPATITIS C (acceda al documento original del CGCOF)
SUMARIO
- Introducción
- Biología del VHC
- Estado actual del tratamiento farmacológico
o Aspectos farmacológicos
o Eficacia y seguridad clínica
o Nuevos antivirales de acción directa frente al VHC
o Protocolos terapéuticos
o ¿Erradicación de la hepatitis C?
- El papel del farmacéutico
- Bibliografía
INTRODUCCIÓN
Se estima que la infección por el virus de la hepatitis C (VHC) afecta a 130-150 millones de personas en todo el mundo (1,8-2,0%), con una incidencia anual de 3-4 millones de nuevos casos1. En España, la prevalencia de la infección por VHC C se sitúa en torno al 1,7% de la población general, lo que supone alrededor de 700.000 personas infectadas, la mayoría aún sin diagnosticar actualmente; de ellas, entre 400.000 y 600.000 desarrollarán hepatitis crónica. En cualquier caso, más del 50% de los pacientes que han necesitado un trasplante de hígado son pacientes con hepatitis C que han evolucionado a una enfermedad hepática terminal.
Generalmente, la infección aguda por VHC es asintomática y muy raramente se asocia a una enfermedad mortal. Entre un 15% y un 45% de las personas inicialmente infectadas eliminan el virus espontáneamente en un plazo de tres a seis meses sin necesidad de tratamiento alguno, pero no parece haber casos de curación espontánea más allá del primer año tras la infección. El restante 55-85% desarrolla hepatitis crónica; de estos, un 70-85% se estabilizan mientras que el 15-30% restante evoluciona a cirrosis hepática a lo largo de un periodo muy variable, que oscila entre 5 y más de 30 años, de los cuales muchos acabarán por padecer un cáncer de hígado (hepatocarcinoma), a un ritmo de un 2% anual.
Las formas más graves y progresivas de hepatitis C aguda acontecen en pacientes trasplantados y en aquellos coinfectados por el virus de la hepatitis B (VHB) o el de la inmunodeficiente humana 1 (VIH-1); de hecho, se estima que entre el 20% y el 25% de los pacientes con VIH están coinfectados por VHC. Según la OMS, entre 300.000 y 500.000 personas mueren anualmente en todo el mundo por enfermedades hepáticas relacionadas con la hepatitis C.
Biología del VHC
El virus de la hepatitis C (VHC) está encuadrado en el género Hepacivirus, que forma parte de la familia Flaviviridae. Se trata de un virus envuelto de un diámetro aproximado de 50 nm; contiene con una única cadena de ARN en sentido positivo (5'-3').
Existen numerosos genotipos y subgenotipos del VHC. En Europa y EEUU el más frecuente es el1 (a y b, 70% de los casos), seguido por el 2 (a y b) y 3 (25%). El 2 y 4 (b, c, e y m) son más frecuentes en África del Norte y Central, y el 6p y 2i en Asia. En particular, en Europa predomina el subgenotipo 1b, seguido de 2a, 2b, 2c y 3a; por su parte, en Norte América predomina el 1a, seguido de 1b, 2a, 2b y 3a. Concretamente, en España30 el genotipo 1b supone 44% de los casos, frente al 26% del 1a, 20% del 3, 8% del 4 y 3% del 2.
Tras la infección aguda y su distribución sanguínea, una vez en el hígado, el VHC utiliza la maquinaria celular del hepatocito para replicarse. La expresión del ARN viral conduce a la síntesis de una única proteína (poliproteína) de gran tamaño (3.011 aminoácidos), que requiere de la acción de varias proteasas para liberar las formas activas de las proteínas virales, que incluyen a tres proteínas estructurales (E) y siete no estructurales (NS). Esta poliproteína (C(F)-E1-E2-p7-NS2-NS3-NS4A-NS4B- NS5A-NS5B) genera al menos diez proteínas maduras al ser procesada por la señal peptidasa del retículo endoplásmico, liberando las proteínas C, E1, E2 y p7 que forman la cápside viral (C) y la envoltura de la partícula (E1 y E2); por su parte, la p7 forma los canales iónicos en la envoltura viral necesarios para la liberación del genoma2.
Por su parte, la región de las proteínas no estructurales (NS2 a NS5B) que participan en la replicación son procesadas por dos enzimas virales: NS2 y NS3 que generan un corte autocatalítico en las regiones NS2-NS3 y NS3-NS4A respectivamente y permiten la formación del complejo serina- proteasa NS3/4A que procesa el resto de la poliproteína viral, provocando la maduración de las proteínas NS4B, NS5A y NS5B con función de polimerasa de ARN dependiente de ARN (NS5B) y de fosfoproteína (NS5A); por el momento, la función de la proteína NS4B no está plenamente comprendida. Estas proteínas NS toman el ARN viral formando un complejo de replicación – sistema replicón – que es asociado a membranas citoplasmáticas modificadas. En este sentido, la capacidad de replicación del VHC es enorme, calculándose en un billón (1012) el número de nuevos virus que son capaces de ser producidos durante un solo día en una persona infectada.
La proteína NS3 del VHC es una enzima multifuncional ya que presenta en el primer tercio de su estructura una actividad de serina-proteasa y en el resto una función de ARN helicasa DexH/D que revierte el enrollamiento de cadenas de ARN formadas durante la replicación viral. El extremo NS4A es una proteína anfipática de 54 aminoácidos que se asocia no covalentemente con las cadenas A0 y A1 de NS3 y provoca una reorganización en su estructura, optimizando así la actividad de proteasa de NS3; además NS4A promueve la localización del complejo NS3/4A en la membrana del retículo endoplásmico donde es procesada la poliproteína viral.
Por su parte la proteína NS5A es una proteína intensamente fosforilada que, una vez escindida de la poliproteína viral, localiza a las membranas donde se une a la fracción 3’-terminal del ARN viral recién sintetizado y participa en la replicación del genoma viral, en parte a través de interacciones con la ARN polimerasa dependiente del ARN viral. Esta última es la NS5B, la cual desarrolla un papel esencial en la replicación del ARN viral, utilizando la cadena de este última como molde para nuevas cadenas y catalizando el proceso de polimerización de los ribonucleótido-trifosfato (rNTP) durante este proceso de replicación. Es responsable de producir la hebra de ARN complementaria – ARN(-) – que servirá de molde para fabricar las auténticas hebras de ARN viral – ARN(+) –, que a su vez podrán ser de nuevo replicados y traducidas, o bien empaquetados en las proteínas estructurales para formar nuevas partículas virales de VHC, que son liberadas mediante un proceso de exocitosis.
El hecho de que el VHC sea un virus ARN implica que su material genético es más inestable que el de los virus ADN, por lo que la tasa de mutaciones es, también, mucho mayor. En este sentido, el VHC posee un elevada variabilidad genética (1.400-1.900 sustituciones/nucleótido/año), debida principalmente a la sustitución nucleotídica que ocurre durante el proceso replicativo y por la falta de actividad de exonucleasa de la polimerasa viral, que impide la corrección de errores en la secuencia replicada. Sin embargo, esta variabilidad no es uniforme, ya que existen regiones altamente conservadas, como la secuencia que codifica para la proteína de la cápside viral (C), la región para la proteasa de serina NS3 y los extremos 5' y 3' no traducibles de la cadena de ARN; mientras que otras regiones, como las que codifican las proteínas NS4B, NS5A y las regiones hipervariables 1 y 2 (RHV-1 y RHV-2) en la proteína de envoltura E2, difieren hasta en más de 50%. Todas estas diferencias en el genotipo del VHC dan origen a las variantes genotípicas virales mencionadas anteriormente.
Estado actual del tratamiento farmacológico
El tratamiento farmacológico de la hepatitis C crónica consistía hasta hace apenas cinco años en la administración de interferón alfa (generalmente, como peginterferón alfa) subcutáneo y ribavirina oral durante 24-72 semanas. Este tratamiento se asocia con una respuesta viral sostenida no demasiado satisfactoria (30-50%) y un perfil notable de efectos adversos3.
En el año 2011 se produjo un cambio notable en el panorama terapéutico de la hepatitis C, al comercializarse el boceprevir (Victrelis®) y el telaprevir (Incivo®) – la primera generación de inhibidores selectivos y reversibles de la proteasa NS3 – para el tratamiento de pacientes infectados por VHC de tipo 1, tanto no tratados previamente (naïve) como tratados, en combinación con peginterferón alfa y ribavirina (terapia triple). En estas circunstancias, las tasas de respuesta tanto en pacientes naïve como en pretratados llegaban a alcanzar hasta un 70% en algunas subpoblaciones de pacientes, permitiendo acortar la duración del tratamiento en algunos casos de 48 a 24 semanas. Sin embargo, boceprevir y telaprevir presentan un perfil toxicológico importante que obliga a suspender el tratamiento en un porcentaje de pacientes netamente superior a los tratados solo con peginterferón alfa y ribavirina, amén de un amplio abanico de interacciones farmacológicas, lo cual, asociado con la propia complejidad del tratamiento, dejaba un amplio margen para la mejora4,5.
Tras esta primera generación de inhibidores de la proteasa del VHC, en 2104 llegó una nueva oleada de agentes con propiedades farmacodinámicas, farmacocinéticas y toxicológicas más satisfactorias. Se trata del simeprevir (Olysio®), inhibidor dual de NS3 y NS4A, del daclatasvir (Daklinza®), inhibidor de la NS5A, y del sofosbuvir (Sovaldi®), inhibidor de la NS5B. Todos ellos fueron autorizados por la Agencia Europea de Medicamentos (EMA, European Medicines Agency) por un procedimiento acelerado, dada la relevancia de su aportación terapéutica.
Aspectos farmacológicos
El boceprevir actúa inhibiendo específicamente la proteasa NS3 implicada en el fraccionamiento de la poliproteína que es codificada por el ARN viral, impidiendo por tanto la replicación del VHC. Concretamente, se une de forma selectiva y reversible al sitio activo de la proteasa NS3 (Ser139), través de un resto cetoamida, bloqueándolo. El grado de capacidad inhibitoria sobre la proteasa NS3 no es igual para todos los genotipos de VHC. En este sentido, es máximo para 1a y 1b, pero es dos veces menor para 3a y tres veces menor para 2a. La resistencia del VHC al boceprevir se asocia a mutaciones únicas localizadas en diferentes posiciones (V36, Q41, F43, T54, Q86, S122, A150, R155, A156, V170 y E176), que reducen en varias veces la sensibilidad al fármaco. La incorporación de una segunda mutación puntual, en especial de la A156T, llega a reducir la sensibilidad en 80 veces. En los estudios clínicos realizados sobre genotipo 1b, la incidencia de cepas variantes resistentes afectó al 15% de los pacientes4.
El telaprevir actúa de forma idéntica al boceprevir. El grado de capacidad inhibitoria del telaprevir sobre la proteasa NS3 es máximo para 1a, 1b y 2, pero es sustancialmente menor para el 3 y el 4. La resistencia del VHC al telaprevir se asocia a mutaciones únicas localizadas en diferentes posiciones (V36, T54 y R155), que reducen entre 3 y 25 veces la sensibilidad al fármaco. Aún mayor resistencia confiere la mutación A156 y la doble sustitución V36+R155, asociada con una reducción de la eficacia del telaprevir de más de 25 veces. En cualquier caso, todas las variantes resistentes al telaprevir mantienen su nivel de sensibilidad al interferón alfa y a la ribavirina5.
El simeprevir actúa inhibiendo específicamente el complejo de serina proteasa NS3/4A, lo que impide la replicación viral. La proteína NS3 del VHC es multifuncional ya que presenta en el primer tercio de su estructura una actividad de serina-proteasa y en el resto función de ARN helicasa DexH/D que revierte el enrollamiento de cadenas dobles de ARN formadas durante la replicación viral. El extremo NS4A es una proteína que se asocia con las cadenas de NS3 y provoca una reorganización en su estructura, optimizando así la actividad de proteasa de NS3; además NS4A promueve la localización del complejo NS3/4A sobre la membrana del retículo endoplásmico donde es procesada la poliproteína viral. El fármaco es especialmente activo frente a los genotipos 1a y 1b (es tres veces más potente bloqueando la proteasa NS3 del 1a que del 1b), aunque también tiene efectos significativos sobre los genotipos 2a, 4a y 6a; por el contrario, la proteasa de los genotipos 3a y 5a es menos susceptible.
La resistencia del VHC a simeprevir está directamente relacionada con mutaciones que conducen a determinadas variaciones en la secuencia peptídica de la proteasa NS3, en particular de los aminoácidos localizados en las posiciones 40, 80, 122, 155, 156 y 168, siendo las más comúnmente descritas como causantes de resistencia clínica al fármaco en pacientes con VHC (no alcanzaron una respuesta virológica sostenida) las mutaciones por sustitución D168E (ácido glutámico por ácido aspártico en la posición 168; 14,5% para pacientes con VHC 1a y 17,4% para 1b), D168V (valina por ácido aspártico; 10,3% en 1a y 60,5% en 1b), Q80R (arginina por glutamina; 4,3% para 1a y 12,3% para 1,b) y R155K (lisina por arginina; 76,7% para 1a y 0% para 1b). En cuanto a la resistencia cruzada, las cepas de VHC infectantes de los pacientes tratados con simeprevir que no experimentaron curación virológica (especialmente, con la mutación R155K) también presentaban una susceptibilidad reducida a telaprevir y boceprevir. No obstante, las variantes resistentes a simeprevir mostraron en general susceptibilidad a los inhibidores de NS5A (daclatasvir, etc.) y, viceversa16.
El daclatasvir actúa inhibiendo específicamente la NS5A, una proteína con diversas funciones relacionadas con la replicación del VHC y el ensamblaje de los viriones. El fármaco se une selectivamente en concentraciones picomolares a la proteína NS5A, alterando su localización subcelular, sus procesos de hiperfosforilación e inhibiendo la síntesis de ARN viral. Cabe recordar que la proteína NS5A es una proteína intensamente fosforilada que, una vez escindida de la poliproteína viral, localiza a las membranas donde se une a la fracción 3’-terminal del ARN viral recién sintetizado y participa en la replicación del genoma viral, en parte a través de interacciones con la ARN polimerasa dependiente del ARN viral (NS5B). A pesar de su extraordinaria actividad frente al VHC, que se manifiesta en prácticamente los genotipos virales más comunes (1a, 1b, 2a, 2b, 3a, 4a, 5a y 6a), el daclatasvir tiene una baja barrera de resistencia a las mutaciones para algunos genotipos, particularmente para 1a, 2a, 2b y 3a, mientras que es bastante más elevada para los genotipos 1b, y 4a. El grado de susceptibilidad (expresado como EC50) de las cepas salvajes (no mutadas) oscila entre 0,003 nM (1b) y 0,26 (3a), lo que implica una diferencia de casi 100 veces en potencia antiviral. La mayoría las mutaciones más resistentes en la NS5A del VHC de genotipo 1a se deben a la sustitución de un solo aminoácido, siendo una de las más peculiares la Q30E (sustitución de glutamina por ácido glutámico en la posición 30), lo que eleva la EC50 a 111 nM, 18.500 veces mayor que en el tipo salvaje (0,006 nM). Otras mutaciones únicas que confieren resistencia a daclatasvir en genotipo 1a son M28T, Q30E, Q30H, Q30R, Q30S, L31M, L31V, Y93C y Y93H, con valores de EC50 entre 1 y 111 nM; algunas mutaciones dobles, como Q30R-L31M y Q30H-Y93H también producen altos niveles de resistencia a al genotipo 1a (EC50 410-868 nM); por el contrario, estas mutaciones – salvo la Q30H-Y93H – no afectan sustancialmente a la sensibilidad al daclatasvir por los VHC de genotipo 1b. La mutación L31M reduce la susceptibilidad al daclatasvir de los genotipos 2a y 2b en 440 y 2.600 veces, respectivamente. La frecuencia de cepas mutadas encontradas17 en pacientes no tratados previamente oscila entre el 1% y el 7% para el genotipo 1a, llegando al 60% en los genotipos 2.
El sofosbuvir actúa inhibiendo específicamente la NS5B, una ARN polimerasa dependiente del ARN viral; esta inhibición impide la replicación del material genético viral. En realidad, el sofosbuvir es un profármaco que requiere ser fosforilado hasta formar el trifosfato, la forma biológicamente activa. Como tal compite con el uridilato por la ARN polimerasa, provocando la finalización prematura del proceso de replicación de la nueva cadena de ARN viral en formación. El sofosbubir es activo sobre los genotipos 1, 2, 3, 4, 5 y 6 del VHC, con valores de la concentración inhibitoria para el
50% (CI50%) que van desde 0,01 a 2,6 µM.
La resistencia del VHC a sofosbuvir está directamente relacionada con mutaciones que conducen a determinadas variaciones en la secuencia peptídica de la ARN polimerasa NSB5, siendo la más comúnmente descrita como causante de una reducida susceptibilidad al fármaco por los VHC la mutación S282T, por sustitución de serina por treonina en la posición 282 de la cadena peptídica. Esta mutación no parece afectar a la susceptibilidad del VHC a otros tipos de antivirales de acción directa2.
Eficacia y seguridad clínica
La adición del boceprevir a la combinación de interferón o peginterferón alfa y ribavirina mejora notablemente la respuesta a estos últimos, cuantificada como respuesta virológica sostenida durante 12 semanas tras finalizar el tratamiento (RVS-12), ampliando entre 20 y 30 puntos porcentuales la respuesta, con una elevada significación tanto estadística como clínica. Por otro lado, los pacientes naïve (no tratados previamente) se benefician de un acortamiento de la duración del tratamiento estándar, pasando de 48 a 28 semanas, con mejora en la eficacia y en la seguridad (se ahorran 20 semanas de tratamiento con interferón alfa y ribavirina). Asimismo, la eficacia de la adición de boceprevir al tratamiento estándar en pacientes parcialmente refractarios a éste o en aquellos que experimentan recidivas tras él, también ha sido robustamente demostrada, lo que amplía sustancialmente el abanico de pacientes potencialmente beneficiados6,7. Desde el punto de vista de la seguridad, el boceprevir supone un incremento significativo de la incidencia de efectos adversos, incluyendo los más graves, si bien la tasa de suspensiones del tratamiento por este motivo no es significativamente diferente del tratamiento estándar. De todos ellos, el principal problema es la anemia, que requiere la administración de epoetina o análogos, con el consiguiente aumento de efectos adversos, de molestias para el paciente y de los costes del tratamiento4.
La eficacia del telaprevir en asociación con peginterferón alfa y ribavirina ha sido demostrada frente a esta combinación (más placebo) en pacientes naïve, con una superioridad manifiesta (respuesta viral sostenida del 75% vs. 44%, lo que permite acortar el tratamiento actual de 48 a 24 semanas en el 60% de los pacientes, aproximadamente8-10. Asimismo, esta superioridad ha sido demostrada con una magnitud similar a la anterior en pacientes previamente tratados con interferón alfa y ribabvirina de forma insatisfactoria (respuesta nula o parcial, o recaída). Además, los resultados han demostrado ser muy consistentes, sin que la superioridad sobre el placebo variase de forma notable considerando los subgenotipos virales (1a o 1b), el grado de daño hepático preexistente o la presencia de cepas variantes (IL28B). La mayoría de fracasos del tratamiento con telaprevir se relacionan con cepas resistentes – con resistencia cruzada, posiblemente, con el boceprevir – sin que se sepa por el momento cuál será su efecto sobre posibles nuevos intentos de tratamiento. No obstante, parece que dichas cepas resistentes revierten a las formas salvajes – sensibles – cuando se suspende el tratamiento con telaprevir.
El telaprevir es un fármaco con una toxicidad importante, con tasas de eventos adversos graves de 6,9%, frente a un 2,9% con placebo. En cualquier caso, la suspensión del tratamiento en los estudios clínicos de referencia fue del 14,2% vs. 4,1%, y hasta un 22% de los pacientes requirieron reducir la dosis de ribavirina cuando se utilizaba telaprevir en combinación, frente a 9% con placebo. Es más relevante aún el riesgo de erupciones exantemáticas graves (5% de grado ≥3), habiéndose descritos varios casos de síndrome de Stevens Johnson. Es muy notable, asimismo, el perfil de interacciones farmacológicas5.
Los resultados de los ensayos clínicos con simeprevir muestran tasas de respuesta viral sostenida a las 12 semanas hasta 40 puntos porcentuales por encima de las conseguidas solo con la terapia doble de peginterferón alfa y ribavirina: 80 vs. 50% en pacientes no tratados anteriormente (naïve), 79 vs. 37% en pacientes tratados y respondedores pero con recaída viral posterior, 76 vs. 9% en parcialmente respondedores e incluso 51 vs. 19% en no respondedores11-13. Los resultados son también satisfactorios en pacientes coinfectados por VIH y VHC. No obstante, es preciso indicar que la eficacia en pacientes infectados por VHC de genotipo 1a y con polimorfismo Q80K es solo marginal con respecto a la terapia doble; este polimorfismo viral es frecuente en el genotipo 1a (19-48%) y se asocia con un cierto grado de resistencia al simeprevir14. Datos adicionales15 aportan resultados muy convincentes asociando simeprevir y sofosbuvir, tanto en pacientes pretratados no respondedores al peginterferón como en naïve y con independencia del nivel de fibrosis hepática.
A diferencia de telaprevir y boceprevir, el simeprevir es un fármaco relativamente bien tolerado, sin que su incorporación a la terapia doble de peginterferón alfa y ribavirina dé lugar a un incremento significativo de la toxicidad general ni obligue a más pacientes a suspender el tratamiento por este motivo. Los eventos adversos descritos con algo más de frecuencia que el placebo son prurito, náusea, exantema, mialgia, etc., y no se ha descrito ningún riesgo especial. También a diferencia de telaprevir y boceprevir, el simeprevir solo requiere una única dosis oral diaria, frente a las tres de aquellos16.
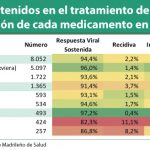
Por su parte, la eficacia de la combinación de daclatasvir con sofosbuvir ha sido claramente demostrada18 en pacientes con genotipo viral 1, 2, 3 y 4, con tasas de respuesta viral sostenida por encima del 90%. En el caso de los genotipos 1a y 1b también se ha demostrado esta misma elevada tasa de respuesta en pacientes que habían experimentado un fallo viral previo a boceprevir o telaprevir. Presenta un perfil de seguridad muy benigno, con efectos adversos inespecíficos (fatiga, cefalea, náusea) y poco intensos17.
En pacientes con VHC de genotipo 1 tratados con sofosbuvir las tasas globales de respuesta virológica sostenida son, en combinación con peginterferón alfa-2a y ribavirina, muy elevadas (90% y 80% en pacientes sin y con cirrosis, respectivamente). Por otro lado, la utilización de pautas de 24 semanas de duración y sin interferón obtiene tasas del 50-70%, superiores a las obtenidas con pautas de interferón y ribavirina de 48 semanas. Por otro lado, se obtienen tasas cercanas al 80% en pacientes coinfectados con VIH utilizando pautas de 12 o 24 semanas de sofosbuvir y ribavirina (con o sin tratamiento previo para el VIH). En infecciones por VHC de genotipo 2, las tasas de respuesta están en torno al 95% en pacientes naïve y del 93% en aquellos inelegibles o intolerantes al interferón, con pautas de sofosbuvir y ribavirina de 12 semanas. Por su parte, en los casos ligados al genotipo 3 se requieren tratamientos de sofosbuvir y ribavirina de 24 semanas de duración, ya que las de 12 semanas producen resultados notablemente inferiores. Por último, los datos correspondientes19,21,23,24-26 a los genotipos 4, 5 y 6 – que son raros en la Unión Europea – son escasos, aunque no parecen diferir sustancialmente de los obtenidos para el genotipo 1.
El sofosbuvir tiene presenta una buena tolerabilidad en combinación con ribavirina, con o sin interferón, sin que se hayan observado efectos adversos específicos del fármaco, mostrando mejor tolerabilidad que el interferón2.
Nuevos antivirales de acción directa frente al VHC
Ya ha sido autorizada por la EMA europea* y la FDA estadounidense la combinación de ledipasvir, un inhibidor de la NS5A, con sofosbuvir (Harvoni®), que ha obtenido excelentes resultados en pacientes con VHC de genotipo 1, tanto en pacientes naïve con tasas de respuesta virológica sostenida del 97-99% con tratamientos de 12 y 24 semanas19 y del 96-99% en pacientes previamente tratados20, e incluso en tratamientos abreviados de 8 semanas de duración22. Asimismo, también hay datos consistentes que apuntan la utilidad en pacientes sometidos a trasplante hepático, algo especialmente relevante; a lo que hay que agregar la utilidad del fármaco en el retratamiento de pacientes no curados anteriormente.
También están autorizados por EMA y FDA paritaprevir, ombitasvir y dasabuvir, que inhiben, respectivamente, la proteasa, la NS5A y la polimerasa. Paritaprevir y ombitasvir se han combinado en una única formulación, asociados a ritonavir† (Viekirax®) y mientras que dasabuvir es formulado independientemente (Exviera®)‡. La combinación de ambas formulaciones ha mostrado tasas de respuesta viral sostenida del 96-100% en pacientes no cirróticos con hepatitis C con VHC de genotipo 1b tratados durante 12 semanas, con independencia del uso de ribavirina; asimismo, se encontraron tasas de respuesta del 95-97% en pacientes infectados con el genotipo 1a. Igualmente, en pacientes con cirrosis se alcanzaron tasas del 92% y en aquellos que no había respondido previamente a peginterferón y ribavirina llegaron a un 89-94%, aunque con 24 semanas de tratamiento27.
* Aunque no comercializada aún es España.
† El ritonavir es utilizado en la combinación solo con fines potenciadores farmacocinéticos de los otros dos agentes antivirales.
‡ No comercializados aún en España.
Finalmente, aún no ha sido comercializada la combinación de grazoprevir (un inhibidor de la proteasa) y elbasvir (inhibidor de la NS5A), que se asocia con una tasa de respuesta viral sostenida del 87-98% en pacientes con hepatitis C mono o coinfectados por VIH, en 12 semanas de tratamiento28. Además de los fármacos citados anteriormente, hay un amplio grupo de agentes antivirales de acción directa activos frente al VHC cuya autorización por la EMA está previsiblemente próxima: asunaprevir (inhibidor de la NS3), vaniprevir (inhibidor dual de NS3 y NS4A) y deleobuvir (inhibidor de la NS5B), etc.
Protocolos terapéuticos
En el estado actual del conocimiento científico es difícil establecer un protocolo definitivo de uso de los diferentes agentes antivirales disponibles para la hepatitis C. La continua y abundante incorporación de nuevos fármacos y de nuevos datos procedentes de los numerosos ensayos clínicos que están finalizando o que están en pleno desarrollo, provoca un cierto grado de incertidumbre a la hora de diseñar el protocolo terapéutico más adecuado a cada situación. Tanto es así, que las guías clínicas quedan desfasadas en cuestión de semanas y, por ello, cualquier pretensión de establecer una guía terapéutica permanente resulta ilusoria. Por si fuera poco, la problemática relacionada con la financiación pública de estos medicamentos eleva la cuestión a un grado notable de complejidad.
En cualquier caso, lo que parece evidente es que la documentación clínica avala la elevada eficacia y el aceptable perfil toxicológico de los nuevos agentes activos simeprevir, daclatasvir, ledispasvir, paritaprevir, ombitasvir, dasabuvir y, en particular, sofosbuvir. Y todo ello sin olvidar a los nuevos fármacos y sus combinaciones que están “asomando” por el horizonte.
El Ministerio de Sanidad, Servicios Sociales e Igualdad de España ha desarrollado29 un Plan Estratégico para el Abordaje de la Hepatitis C en el Sistema Nacional de Salud, en el que se contemplan cuatro líneas estratégicas fundamentales: cuantificar la magnitud del problema, determinar las características epidemiológicas de los pacientes y establecer medidas preventivas; definir una estrategia terapéutica con los fármacos antivirales de acción directa; establecer mecanismos de coordinación y fomentar el avance del conocimiento de la prevención, el diagnóstico y el tratamiento de la hepatitis C.
Uno de los criterios fundamentales en la estrategia terapéutica es considerar el nivel de fibrosis hepática que presenta el paciente en el momento del diagnóstico, que determina la potencial utilidad de los tratamientos disponibles. Cabe recordar que la fibrosis hepática implica la acumulación de tejido cicatricial en el hígado, con acumulación progresiva de fibras de colágeno en su parénquima y cuyo estadio final es la cirrosis. La progresión de la fibrosis hepática altera la estructura normal del hígado, lo que da lugar – entre otros muchos y diversos problemas – a trastornos en su circulación con aumento de la presión de la vena porta abdominal y cuando este aumento es importante conduce a la aparición de varices esofágicas, retención de agua, con edemas en miembros inferiores y ascitis, que comprometen la vida del paciente.
Se suele cuantificar el nivel de fibrosis hepática mediante Fibroscan, una técnica
ultrasonográfica no invasiva basada en la elastografía, que mide la velocidad de propagación de ondas elásticas a través del hígado. Valores menores de 7 kPa (kiloPascal), equivalen a niveles 0 y 1 de fibrosis de la biopsia hepática (F0 y F1); la fibrosis es moderada entre 7 a 9,4 kPa (F2); valores entre 9,4 y 12 kPa indican una fibrosis avanzada (F3) y por encima de 12 kPa, la fibrosis es grave (F4), típicamente cirrosis. En caso de ausencia de biopsia o Fibroscan, se consideran otros factores, tales como la presencia de varices esofágicas o ascitis, contemplándose la posibilidad de diagnóstico por imagen mediante TAC (tomografía axial computadorizada) o RMN (resonancia magnética nuclear).
La Estrategia propone tratar con los nuevos antivirales a pacientes tanto monoinfectados como coinfectados con el VIH:
- Pacientes con fibrosis hepática significativa (F2 a F4) con independencia de la existencia o no de complicaciones previas a la hepatopatía.
- Pacientes en lista de espera de trasplante hepático o trasplantados (hepáticos que hayan vuelto a infectarse y no hepáticos con hepatitis C).
- Pacientes que no hayan respondido a la triple terapia con inhibidores de la proteasa de primera generación.
- Pacientes con hepatitis C con manifestaciones extrahepáticas clínicamente relevantes del virus de la hepatitis C, sea cual sea el grado de fibrosis.
- En cualquier caso, y también con independencia del grado de fibrosis, se debe indicar el tratamiento en pacientes con elevado riesgo de trasmisión y mujeres en edad fértil que deseen un embarazo.
- Genotipo 1. Cualquiera de los siguientes regímenes (no hay datos comparativos entre ellos):
o Pacientes previamente no tratados (naïve) o con recaída tras un éxito inicial con terapia triple (INF+RBV+boceprevir o telaprevir)§
SOF+SIM ± RBV
SOF+DAC ± RBV
SOF+LED ± RBV
PER/RIT+DAS+OMB ± RBV
o Pacientes con fracaso previo a terapia triple
SOF+SIM+RBV
SOF+LED+RBV
SOF+DAC+RBV
- Genotipo 2:
- Genotipo 3:
- Genotipo 4:
SOF+RBV
SOF+RBV+IFN (si se tolera)
SOF+LED+RBV
SOF+RBV+IFN (cirróticos que no hayan respondido anteriormente)
SOF+DAC (solo pacientes con nivel F2 y F3)
o Pacientes previamente no tratados (naïve) o con recaída tras un éxito inicial con terapia triple (INF+RBV+boceprevir o telaprevir)
SOF+LED
PAR/RIT+OMB+RBV (pacientes no cirróticos)
SOF+RBV
SOF+SIM
o Pacientes no respondedores a terapia triple:
SOF+SIM±RIB
SOF+LED±RIB
- DAC= Daclatasvir; DAS= Dasabuvir; IFN= Interferón (peginterferón) alfa 1a; LED= Ledipasvir; OMB= Ombitasvir; PAR= Paritaprevir; RBV= Ribavirina; RIT= Ritonavir; SIM= Simeprevir; SOF= Sofosbuvir.
PAR/RIT+OMB+RBV (pacientes no cirróticos)
SOF+RBV
- Genotipos 5 y 6: Son de muy baja prevalencia en España, por lo que su tratamiento debe ser
individualizado, aunque podrían ser tratados de forma similar al genotipo 1.
- Pacientes con cirrosis y con requerimiento de trasplante hepático:
SOF+SIM±RIB
SOF+DAC±RIB
SOF+LED±RIB
PAR/RIT+OMB+RBV
- Pacientes transplantados hepáticos con recidiva:
o Genotipo 1:
SOF+SIM±RIB
SOF+DAC±RIB
SOF+LED±RIB
PAR/RIT+OMB+RBV
o Genotipo 2: SOF+RBV
o Genotipo 3:
SOF+LED±RIB
SOF+DAC±RIB
o Genotipo 4:
SOF+SIM±RIB
SOF+LED±RIB
PAR/RIT+OMB+RBV
¿Erradicar la hepatitis C?
Con la llegada de los nuevos agentes antivirales, se ha especulado con la posibilidad de que la hepatitis C pudiera llegar a ser erradicada. De hecho, hay argumentos sólidos que pueden sustentar este objetivo: se dispone de medicamentos con muy altas tasas de eliminación viral, no existen reservorios para el VHC además del hombre y la cadena de transmisión es perfectamente conocida (intravenosa y sexual) y puede ser interferida satisfactoriamente.
Sin embargo, frente a los anteriores argumentos existen otros no menos consistentes: una parte importante de los pacientes (la mayoría, en los países en vías de desarrollo) desconocen su condición de infectados, los tratamientos potencialmente erradicadores no son asequibles más que para una minoría localizada fundamentalmente en los países desarrollados ( y ello con limitaciones) y hasta un 15% de los pacientes virológicamente curados vuelven a reinfectarse por el VHC30, porcentaje que algunos investigadores31 elevan hasta el 23%. Esto puede ilustrarse con el ejemplo de la sífilis, que sigue siendo una de las enfermedades de transmisión sexual más prevalentes en el mundo, a pesar de que se dispone de fármacos eficaces, seguros y que cuestan apenas unos pocos céntimos por tratamiento.
En definitiva, la erradicación de una enfermedad infecciosa no solo necesita de una eficaz estrategia sanitaria multifactorial y multinacional, y de una importante aportación financiera; también requiere una voluntad política y social globalizada que lo defina como un objetivo prioritario e irrenunciable.
El papel del farmacéutico
Los nuevos medicamentos antivirales directos activos sobre el VHC han sido calificados administrativamente para su dispensación exclusiva en los servicios de farmacia hospitalaria, a pesar de que su uso por los pacientes es, en su inmensa mayoría, extrahospitalario. Ninguno de estos medicamentos requieran medidas especiales de control, como la monitorización continua durante la administración o tras ésta, única justificación clínica que soportaría la exclusividad de uso intrahospitalario de un medicamento**, más allá de los formatos diseñados específicamente para un manejo más conveniente por la farmacia hospitalaria. Es más, todos los nuevos fármacos antivirales activos sobre VHC son de administración oral (muchos solo requieren una única dosis diaria), lo que hace particularmente sencilla su administración por el propio paciente.
Sin embargo, los datos de eficacia y de seguridad ofrecidos por los ensayos clínicos proceden de grupos de pacientes estrechamente controlados a nivel clínico. Para alcanzar los elevados niveles de eficacia y de seguridad referidos se requiere, en la práctica cotidiana, tratar de proyectar esos controles y hacerlos asequibles y personalizados para cada paciente. En definitiva, los farmacéuticos comunitarios pueden colaborar activamente para la consecución de dichos objetivos, promoviendo medidas de prevención y educación sobre la reducción de la transmisión del VHC, mejorar la adherencia a la medicación, ayudar en el seguimiento de los efectos clínicos y adversos, recomendar estrategias de tratamiento para minimizar los efectos adversos e interacciones medicamentosas, y facilitar la disponibilidad de los medicamentos, implicándose en la sostenibilidad del sistema de salud32.
Es especialmente importante tener en cuenta que para aumentar las tasas de adherencia al tratamiento y de cumplimentación total del mismo, se requiere un enfoque centrado en el paciente que se ocupe de sus necesidades de apoyo social, prácticas y emocionales de los pacientes y las estrategias adaptativas de afrontamiento33. Por otro lado, el control de las posibles interacciones clínicamente más relevantes de los antivirales de acción directa sobre el VHC es un aspecto que requiere un especial cuidado y atención personalizada, sobre todo teniendo en cuenta que muchas de dichas interacciones se producen con medicamentos de uso habitual fuera del entorno hospitalario e, incluso que no requieren prescripción médica. En este sentido, un reciente estudio34 realizado sobre 4.251 pacientes con hepatitis C ha mostrado que la prevalencia de interacciones clínicamente relevantes de los tratamientos conteniendo simeprevir o sofosbuvir fueron del 12,6% y 4,7%, respectivamente. Pero tan importante como esto es que el único factor predictor relacionado con los tratamientos fue el uso de 6 o más medicamentos por el paciente en su propio hogar.
La localización de la oficina de farmacia, más próxima al paciente y, en muchos casos, el conocimiento personal del paciente por parte del farmacéutico comunitario, puede facilitar un seguimiento más estrecho del plan de gestión y de minimización de riesgos de los medicamentos, incluyendo la comunicación de sospecha de reacciones adversas por los propios pacientes. Cuando no se trata de una situación de urgencia o emergencia, para el paciente es más fácil, cómodo y rápido acudir a una oficina de farmacia – abierta durante un amplio horario y con guardias periódicas – que a la consulta del médico especialista, necesariamente sujeta a planificación. Todo ello, sin perjuicio – obviamente – de los necesarios controles médicos que cada paciente requiera. En última
instancia, la farmacovigilancia y el seguimiento farmacoterapéutico desde la oficina de farmacia no es una alternativa al seguimiento clínico directo por parte del médico prescriptor, sino un complemento de este seguimiento, que permite optimizar la gestión del control farmacoterapéutico, adaptándose a las necesidades y circunstancias específicas de cada paciente y dándole un valor añadido a los recursos asistenciales sanitarios, tanto en el ámbito público como en el privado.
** Así como las indicaciones dirigidas específicamente para intervenciones necesariamente intrahospitalarias (anestesia, sedación, etc.) o para soporte vital en este entorno clínico.
Bibliografía
- Organización Mundial de la Salud. Nota descriptiva 164. Hepatitis C. Abril 2014. http://www.who.int/mediacentre/factsheets/fs164/es/
- Cuéllar Rodríguez S, 2014. Sofosbuvir (Sovaldi®) en hepatitis C. Panorama Actual Med 2014; 38(377): 835-40
- Webster DP, Klenerman P, Dusheiko GM. Hepatitis C. Lancet. 2015 Feb 13. pii: S0140-6736(14)62401-6. doi: 10.1016/S0140- 6736(14)62401-6.
- Cuéllar Rodríguez S. Boceprevir (Victrelis®) en hepatitis C. Panorama Actual Med 2011; 35(349): 1054-60.
- Cuéllar Rodríguez S. Telaprevir (Incivo®) en hepatitis C. Panorama Actual Med 2012; 36(351): 144-53.
- Bacon BR, Gordon SC, Lawitz E, Marcellin P, Vierling JM, Zeuzem S, et al; HCV RESPOND-2 Investigators. Boceprevir for previously treated chronic HCV genotype 1 infection. N Engl J Med. 2011; 364(13): 1207-17.
- Poordad F, McCone J Jr, Bacon BR, Bruno S, Manns MP, Sulkowski MS, et al; SPRINT-2 Investigators. Boceprevir for untreated chronic HCV genotype 1 infection. N Engl J Med. 2011; 364(13): 1195-206.
- Jacobson IM, McHutchison JG, Dusheiko G, Di Bisceglie AM, Reddy KR, Bzowej NH, et al. ; ADVANCE Study Team. Telaprevir for previously untreated chronic hepatitis C virus infection. N Engl J Med. 2011; 364(25): 2405-16.
- Sherman KE, Flamm SL, Afdhal NH, Nelson DR, Sulkowski MS, Everson GT, et al.; ILLUMINATE Study Team. Response-guided telaprevir combination treatment for hepatitis C virus infection. N Engl J Med. 2011; 365(11): 1014-24.
- Zeuzem S, Andreone P, Pol S, Lawitz E, Diago M, Roberts S; REALIZE Study Team. Telaprevir for retreatment of HCV infection. N Engl J Med. 2011; 364(25): 2417-28.
- Forns X, Lawitz E, Zeuzem S, Gane E, Bronowicki JP, Andreone P, et al. Simeprevir with peginterferon and ribavirin leads to high rates of SVR in patients with HCV genotype 1 who relapsed after previous therapy: a phase 3 trial. Gastroenterology. 2014; 146: 1669- 79.e3. doi: 10.1053/j.gastro.2014.02.051.
- Jacobson IM, Dore GJ, Foster GR, Fried MW, Radu M, Rafalsky VV, et al. Simeprevir with pegylated interferon alfa 2a plus ribavirin in treatment-naïve patients with chronic hepatitis C virus genotype 1 infection (QUEST-1): a phase 3, randomised, double-blind, placebo-controlled trial. Lancet. 2014; 384(9941): 403-13. doi: 10.1016/S0140-6736(14)60494-3.
- Manns M, Marcellin P, Poordad F, de Araujo ES, Buti M, Horsmans Y, et al. Simeprevir with pegylated interferon alfa 2a or 2b plus ribavirin in treatment-naive patients with chronic hepatitis C virus genotype 1 infection (QUEST-2): a randomised, double-blind, placebo-controlled phase 3 trial. Lancet. 2014; 384(9941): 414-26. doi: 10.1016/S0140-6736(14)60538-9.
- Poveda E, Wyles DL, Mena A, Pedreira JD, Castro-Iglesias A, Cachay E. Update on hepatitis C virus resistance to direct-acting antiviral agents. Antiviral Res. 2014; 108C: 181-191. doi: 10.1016/j.antiviral.2014.05.015.
- Lawitz E, Sulkowski MS, Ghalib R, Rodriguez-Torres M, Younossi ZM, Corregidor A, et al. Simeprevir plus sofosbuvir, with or without ribavirin, to treat chronic infection with hepatitis C virus genotype 1 in non-responders to pegylated interferon and ribavirin and treatment-naive patients: the COSMOS randomised study. Lancet. 2014 Jul 26. pii: S0140-6736(14)61036-9. doi: 10.1016/S0140- 6736(14)61036-9.
- Cuéllar Rodríguez S. Simeprevir (Olysio®) en hepatitis C. Panorama Actual Med 2014; 38(376): 734-40.
- Cuéllar Rodríguez S. Daclatasvir (Daklinza®) en hepatitis C. Panorama Actual Med 2015; 39(380): 49-53.
- Sulkowski MS, Gardiner DF, Rodriguez-Torres M, Reddy KR, Hassanein T, et al; AI444040 Study Group. Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection. N Engl J Med 2014; 370(3): 211-21. doi: 10.1056/NEJMoa1306218.
- Afdhal N, Zeuzem S, Kwo P, Chojkier M, Gitlin N, Puoti M, et al; ION-1 Investigators. Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection. N Engl J Med 2014; 370(20): 1889-98. doi: 10.1056/NEJMoa1402454.
- Afdhal N, Reddy KR, Nelson DR, Lawitz E, Gordon SC, Schiff E, et al; ION-2 Investigators. Ledipasvir and sofosbuvir for previously treated HCV genotype 1 infection. N Engl J Med 2014; 370(16): 1483-93. doi: 10.1056/NEJMoa1316366.
- Jacobson IM, Gordon SC, Kowdley KV, Yoshida EM, Rodriguez-Torres M, Sulkowski MS, at el; POSITRON Study; FUSION Study. Sofosbuvir for hepatitis C genotype 2 or 3 in patients without treatment options. N Engl J Med 2013; 368(20): 1867-77. doi: 10.1056/NEJMoa1214854.
- Kowdley KV, Gordon SC, Reddy KR, Rossaro L, Bernstein DE, Lawitz E, Shiffman ML, el al; ION-3 Investigators. Ledipasvir and sofosbuvir for 8 or 12 weeks for chronic HCV without cirrhosis. N Engl J Med. 2014; 370(20): 1879-88. doi: 10.1056/NEJMoa1402355.
- Lawitz E, Mangia A, Wyles D, Rodriguez-Torres M, Hassanein T, Gordon SC, et al. Sofosbuvir for previously untreated chronic hepatitis C infection. N Engl J Med 2013; 368(20): 1878-87. doi: 10.1056/NEJMoa1214853.
- Lawitz E, Sulkowski MS, Ghalib R, Rodriguez-Torres M, Younossi ZM, Corregidor A, et al. Simeprevir plus sofosbuvir, with or without ribavirin, to treat chronic infection with hepatitis C virus genotype 1 in non-responders to pegylated interferon and ribavirin and treatment-naive patients: the COSMOS randomised study. Lancet 2014; 384(9956): 1756-65. doi: 10.1016/S0140-6736(14)61036-9.
- Sulkowski MS, Naggie S, Lalezari J, Fessel WJ, Mounzer K, Shuhart M, et al; PHOTON-1 Investigators. Sofosbuvir and ribavirin for hepatitis C in patients with HIV coinfection. JAMA 2014; 312(4):353-61. doi: 10.1001/jama.2014.7734.
- Zeuzem S, Dusheiko GM, Salupere R, Mangia A, Flisiak R, Hyland RH, et al; VALENCE Investigators. Sofosbuvir and ribavirin in HCV genotypes 2 and 3. N Engl J Med. 2014; 370(21): 1993-2001. doi: 10.1056/NEJMoa1316145.
- Klibanov OM, Gale SE, Santevecchi B. Ombitasvir/Paritaprevir/Ritonavir and Dasabuvir Tablets for Hepatitis C Virus Genotype 1 Infection. Ann Pharmacother 2015, Feb 13. pii: 1060028015570729.
- Lawitz E, Gane E, Pearlman B, Tam E, Ghesquiere W, Guyader D, et al. Efficacy and safety of 12 weeks versus 18 weeks of treatment with grazoprevir (MK-5172) and elbasvir (MK-8742) with or without ribavirin for hepatitis C virus genotype 1 infection in previously untreated patients with cirrhosis and patients with previous null response with or without cirrhosis (C-WORTHY): a randomised, open-label phase 2 trial. Lancet. 2014 Nov 11. pii: S0140-6736(14)61795-5. doi: 10.1016/S0140-6736(14)61795-5.
- Rodés J, Albillos A, Andreu AL, Buti M, Crespo J, Moreno A, Zulaika D; Ministerio de Sanidad, Servicios Sociales e Igualdad. Plan Estratégico para el abordaje de la hepatitis C en el Sistema Nacional de Salud (2015).
- Wandeler G, Dufour JF, Bruggmann P, Rauch A. Hepatitis C: a changing epidemic. Swiss Med Wkly. 2015 Feb 6; 145:w14093. doi: 10.4414/smw.2015.14093.
- Hill A. Effects of sustained virological response on the risk of liver transplant, hepatocellular carcinoma, death and re-infection: meta- analysis of 129 studies in 34.563 patients with hepatitis C infection. AASDL; Boston, USA; 10th November 2014 [Abstract 44].
- Mohammad RA, Bulloch MN, Chan J, Deming P, Love B, Smith L, Dong BJ. Provision of clinical pharmacist services for individuals with chronic hepatitis C viral infection: Joint Opinion of the GI/Liver/Nutrition and Infectious Diseases Practice and Research Networks of the American College of Clinical Pharmacy. Pharmacotherapy. 2014; 34(12): 1341-54. doi: 10.1002/phar.1512.
- Sublette VA, Smith SK, George J, McCaffery K, Douglas MW. The Hepatitis C treatment experience: Patients' perceptions of the facilitators of and barriers to uptake, adherence and completion. Psychol Health. 2015 Feb 23: 1-18.
34. Patel N, Nasiri M, Koroglu A, Bliss S, Davis M, McNutt LA, Miller C. A Cross-Sectional Study Comparing the Frequency of Drug Interactions After Adding Simeprevir- or Sofosbuvir-Containing Therapy to Medication Profiles of Hepatitis C Monoinfected Patients. Infect Dis Ther. 2015 Jan 28. [Epub ahead of print]





















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: