Documento de la Organización Médica Colegial: Acceso a los nuevos medicamentos. El ejemplo de la Hepatitis C. Costes, precios y patentes
Fernando Lamata, Ramón Gálvez, Pedro Pita Barros, Javier Sánchez Caro Madrid, 18/6/2015
AGRADECIMIENTOS: Los autores agradecen a todas las personas que han leído el manuscrito proponiendo modificaciones y aclaraciones. También agradecen el trabajo de grupos de investigadores, asociaciones de pacientes, organizaciones no gubernamentales y organismos internacionales que promueven el acceso de los medicamentos necesarios y efectivos para todas las personas que los necesiten, en todo el mundo.
LOS AUTORES: Fernando Lamata es médico especialista en psiquiatría, experto en política y gestión sanitaria. Ha trabajado más de 25 años en la dirección de programas y servicios de salud de ámbito regional y nacional.
Ramón Gálvez es médico especialista en neurología, experto en gestión sanitaria y dirección hospitalaria. Ha trabajado más de 25 años en la dirección de hospitales y en la planificación y gestión de servicios de salud.
Pedro Pita Barros es Vice-Rector y Profesor de Economía en la Universidad Nueva de Lisboa, experto en economía de la salud. Es editor del “International Journal of Health Care Finance and Economics”.
Javier Sánchez-Caro es jurista, Letrado de la Seguridad Social y experto en Derecho Sanitario. Fue responsable de la Asesoría Jurídica del Instituto Nacional de la Salud y Director de la Unidad de Bioética y Orientación sanitaria de la Consejería de Sanidad de la Comunidad de Madrid.
ACCESO A LOS NUEVOS MEDICAMENTOS: EL EJEMPLO DE LA HEPATITIS C. COSTES, PRECIOS Y PATENTES.
INDICE
Resumen. (p.4)
1.El dilema entre el acceso a medicamentos necesarios y el beneficio de las empresas farmacéuticas. El ejemplo de la Hepatitis C. (p.6)
2.¿Cómo se calculan los precios? (p.12)
3.¿Cuál es el coste, cuál es el precio y cuál sería un precio razonable de un medicamento innovador? (p.17)
4. La espiral de precios de los nuevos medicamentos. El ejemplo de los medicamentos oncológicos. (p.22)
5.El sistema de patentes. (p.26)
6.La fijación de precios de los medicamentos en España. (p.31)
7.La fijación de precio a partir de una estimación del “valor”. (p.33)
8.La financiación de la investigación. (p.37)
9.La estrategia de algunas empresas en relación con las patentes y los precios. (p.42)
10.Un mercado atractivo para los inversores. (p.44)
11.¿Qué pueden (y deben ) hacer los gobiernos, los Parlamentos y los demás agentes sociales? (p.45)
12.Conclusiones. (p.50)
13.Recomendaciones. (p.53)
14.Referencias. (p.56)
Acceder al documento completo en formato pdf
RESUMEN Por primera vez en los países llamados de “altos ingresos” se ha negado el acceso a un medicamento, por causa de su precio, a un grupo muy numeroso de pacientes (en la Unión Europea a varios millones de personas). Las personas afectadas han hecho llegar su voz a los Gobiernos, a los Tribunales de Justicia y al Parlamento Europeo exigiendo el derecho a la atención sanitaria que necesitan. El problema de la “barrera del precio”, que ya sufrían los países de ingresos medios y bajos para tratar diversas enfermedades, hace que muchos pacientes no puedan acceder a los medicamentos, o que los sistemas de salud soporten un gasto tan alto que pone en riesgo la funcionalidad y estabilidad de los mismos en el medio y largo plazo. El hecho cierto es que los elevados precios de los nuevos antivirales para la Hepatitis C, medicamentos que han sido incluidos en la lista de medicamentos “esenciales” por la OMS, han llamado la atención sobre el modelo con el que se establecen los precios de los medicamentos. Tal parece que se ha roto un equilibrio que es preciso recuperar.
El precio de un producto se sitúa entre dos extremos: por un lado, el coste de producción; por otro lado, el precio más alto que esté dispuesto a pagar un consumidor, lo que se denomina precio por el “valor” del producto. Los consumidores (en este caso los pacientes y los sistemas de salud) quieren el primer precio, más bajo; las empresas productoras quieren el segundo, más alto. Este es el dilema.
En un mercado libre, si el fabricante fija el precio más alto, poco a poco la competencia hará que el precio tienda a acercarse al coste de producción (como ocurre con los medicamentos genéricos y biosimilares). Pero la concesión de patentes impide la competencia. La justificación formal para que los Gobiernos concedan patentes es la de incentivar la inversión en investigación e innovación, garantizando a la empresa innovadora la recuperación de los costes y la obtención de un beneficio razonable; por lo tanto, el precio fijado bajo la protección de la patente, debería cubrir dichos costes y nada más. Si se fijara un precio más elevado, se estaría haciendo una utilización abusiva de la patente en contra de los derechos de las personas y de la sociedad que otorgó ese privilegio; se rompería el equilibrio en perjuicio del conjunto de la sociedad y de los pacientes.
El argumento de la industria para fijar precios muy altos es el alto coste de la investigación; pero ese coste, según estudios independientes, no justifica de ninguna manera los elevadísimos precios fijados. Por otro lado, los procedimientos de fijación de precios permiten a las compañías no desvelar los costes de producción. En cambio, promocionan el valor creado para el paciente como referencia frente a la cual se debe definir el precio.
Para recuperar el equilibrio roto entre, por un lado el interés del paciente y la sociedad, y por otro lado el interés de algunas industrias farmacéutica (o, en su caso, lo fondos de inversión propietarios de las mismas) proponemos una serie de recomendaciones encaminadas a garantizar a los ciudadanos el acceso a los nuevos medicamentos; estas recomendaciones se pueden resumir en tres: 1) la reducción de los precios de los medicamentos innovadores mediante negociación con la industria, ajustándolos a los costes reales, incluyendo los coses de Investigación y Desarrollo; 2) la posibilidad de establecer licencias obligatorias para aquellos casos donde no se produjera un acuerdo razonable; 3) el diseño e implantación de mecanismos para garantizar la investigación y
el desarrollo de nuevos medicamentos, entre los que se puede valorar la separación de la financiación de la I+D del precio de los medicamentos, mediante mecanismos de coordinación y fondos globales destinados a este fin, en el ámbito de la Unión Europea o Mundial (Organización Mundial de la Salud). Si no cambiamos con urgencia el actual sistema de fijación de precios de los medicamentos se pueden crear graves problemas en el acceso a la atención sanitaria para todos, en todo el mundo.
- El dilema entre el acceso a medicamentos necesarios y el beneficio de las empresas farmacéuticas. El ejemplo de la Hepatitis C.
La importancia de los medicamentos está clara para todos, sobretodo cuando un medicamento nos ha salvado la vida a nosotros o a algún familiar. Los medicamentos bien utilizados (vacunas, antibióticos, analgésicos, antidiabéticos, etc.) contribuyen al mantenimiento y recuperación de la salud.
La atención sanitaria adecuada a las necesidades de la persona, y a las posibilidades de cada país y cada momento es una condición para la garantía del derecho a la salud y la dignidad de los seres humanos. En este momento, en Europa y en todo el planeta, están muriendo personas por falta de acceso al medicamento que necesitan. En este momento muchas personas ven cómo se deteriora su salud, sin poder paliar su sufrimiento, porque ellos o sus sistemas sanitarios no tienen medios para pagar los altos precios de los medicamentos. Para estas personas el tiempo cuesta mucho. Por eso este debate sobre acceso a los medicamentos debe acelerarse y lograr soluciones sin demora. Cuesta vidas.
Los nuevos medicamentos en el contexto del Sector Farmacéutico mundial.
Al mismo tiempo, el Sector Farmacéutico es un sector económico importante. En 2013 el gasto en medicamentos en todo el mundo ascendió a 989.000 millones de dólares. Ahora supera el billón anual y en 2018 está previsto un gasto de 1,3 billones de dólares (IMS 2014). Este aumento se deberá, en los países de ingresos altos, a los nuevos medicamentos de altos precios; mientras que en los países de ingresos medios y bajos, se deberá sobretodo al aumento de cobertura hacia la universalización sanitaria. El gasto farmacéutico es desigual en el mundo: América del Norte y Europa, con un 14% de la población gastan el 61% del total mundial.
Esta diferencia se explica en parte por el acceso universal a la sanidad, pero también a los precios más altos de los nuevos medicamentos que se utilizan más en los países de mayores ingresos. Por otra parte, también se observan importantes diferencias en el gasto en medicamentos entre países de la Unión Europea.
Dinamarca destina un 0,7% del PIB para medicamentos, mientras que España o Italia destinan un 1,5% del PIB, y Portugal o Bélgica destinan un 1,8% del PIB.
Estas diferencias se observan también si comparamos el Gasto Farmacéutico por persona. En Bélgica dicho gasto asciende a 550 € por persona (a paridad de poder adquisitivo), mientras que en Dinamarca es suficiente con 195 € PPA.
Dicho de otra forma, si España gastara lo mismo que Dinamarca en medicamentos / habitante, se ahorraría un 40%.
Las diferencias de gasto farmacéutico por persona pueden reflejar diferentes situaciones en relación con la cobertura (población asegurada), cartera de servicios, tipo de medicamentos financiados, etc. (Danzon P and Pauly M 2002). En todo caso, estas diferencias muestran distintos enfoques de política sanitaria y farmacéutica, en la aprobación de medicamentos, la financiación pública, los copagos, la fijación de precios, la prescripción y la utilización de los medicamentos, que tienen trascendencia tanto para la salud de las personas como para la estabilidad económica de los sistemas de salud.
También se pueden observar diferencias en el consumo de los diferentes tipos de medicamentos entre distintos países (OECD 2014-2). Por ejemplo, en medicamentos antihipertensivos, el consumo medido en Dosis Diarias Definidas por 1000 habitantes varía entre 191 en Austria y 567 en Alemania. La media de la UE18 es 357, mientras que Portugal consumió 252 y España 270. La misma variabilidad se observa en consumo de antidepresivos; la media de la UE18 fue 56, mientras que en Estonia fueron 21 DDD / 1000 habitantes, en España 64 y en Portugal 85. En consumo de antidiabéticos se observan diferencias similares; desde las 39 DDD / 1000 habitantes de Austria hasta las 85 de Finlandia, pasando por 61 en Portugal y 66 en España. Es decir, diferencias de más del doble de DDD por persona entre los diferentes países de la UE.
¿Se pueden explicar estas diferencias por la distinta incidencia y prevalencia de los trastornos? ¿Influyen otras variables, como la práctica médica? Al mismo tiempo se observa un aumento general del consumo de medicamentos entre 2000 y 2012. Para los grupos de medicamentos estudiados el consumo en DDD / 1000 habitantes ha aumentado en casi el doble (antidepresivos y antidiabéticos), el doble (antihipertensivos) o el triple (hipolipemiantes).
En este contexto, muy dinámico, la introducción de nuevos medicamentos de precios muy altos está suponiendo fuertes tensiones que se traducen en desigualdades de acceso a los medicamentos por diferentes países o grupos de población, así como en dificultades presupuestarias para los sistemas de salud.
Los nuevos medicamentos para el tratamiento de la Hepatitis C.
Durante los últimos años se han desarrollado nuevos medicamentos para el tratamiento de la infección con el virus de la hepatitis C. Estos antivirales, según los datos disponibles hasta el momento, son más efectivos, más seguros y con menos efectos secundarios. Tan es así que la Organización Mundial de la Salud los ha incluido en su “Lista de Medicamentos Esenciales” publicada el pasado día 8 de mayo (WHO 2015) Si el tratamiento con estos medicamentos pudiera llegar a toda la población afectada (185 millones de personas están infectadas en el mundo), se podrían evitar miles de muertes prematuras (700.000 al año) y se podría erradicar la enfermedad. De ahí que el Editorial de Lancet de 21 de marzo 2015 se preguntara: “Hepatitis C, ¿sólo a un paso de su erradicación?” (The Lancet 2015).
Es preciso reconocer el trabajo de miles de profesionales sanitarios, de investigadores, de centros sanitarios y laboratorios, que han hecho posible estos avances. El reto ahora es poner a disposición de los pacientes estos tratamientos innovadores. La barrera de acceso es el precio. A veces se dice que la barrera es el coste, pero no es exacto. La dificultad de financiación de estos medicamentos no está en el coste de fabricación sino el precio que ponen los fabricantes, que puede ser 20, 30 y hasta 100 veces lo que cuesta el producto. Ese precio no se justifica por los costes de la investigación. Es un precio que se fija según las estimaciones que hacen las empresas de cuánto pueden pagar los pacientes o los aseguradores públicos o privados y responde a diversas escenarios financieros de las empresas afectadas. Este mecanismo de fijación de precios hace que estos tratamientos no puedan llegar a los miles de pacientes que los necesitan en España, en Europa y en todo el mundo.
El IMS Institute for Healthcare Informatics estima que entre 2013 y 2018 se producirá un gasto anual de 31.000 millones de dólares con estos tratamientos para la Hepatitis C, presentando la mayor tasa de aumento de gasto de todos los grupos de medicamentos en este periodo (IMS 2014). Pero este gasto, aún siendo muy elevado, solo permitiría atender a una pequeña parte de las personas afectadas, debido a los elevados precios.
El problema que nos ocupa, pues, es un conflicto entre dos intereses. Por un lado el interés del conjunto de la sociedad y de los pacientes y, por otro lado, el interés de unas empresas, de sus accionistas y de sus directivos, que quieren obtener el máximo beneficio en el plazo más corto posible. Este es el dilema.
Las compañías farmacéuticas pueden racionalizar eventualmente los altos precios y elevados beneficios como fondos necesarios para investigaciones futuras. Pero aunque esta fuera su intención y el valor de la innovación fuera importante para los pacientes, no se garantiza un buen equilibrio, ya que precios demasiado altos pueden llevar a un desplazamiento de gastos necesarios en otras áreas y para otros pacientes.
El caso “Sovaldi” (sofosbuvir) ha puesto el foco en el desequilibrio que se ha generado en la sociedad y en los sistemas de salud con los precios de los nuevos medicamentos. Ya venían fijándose precios muy altos para otros medicamentos de nueva generación, utilizados en el tratamiento del cáncer o para otras enfermedades neurológicas, cardiovasculares, inflamatorias, etc. Y los precios previstos para los nuevos medicamentos que están actualmente en fase de desarrollo por las compañías farmacéuticas plantearán el mismo problema. No es el problema de un solo producto, es el problema, como veremos más adelante, del modo de compensar la innovación.
Lo cierto es que estos otros casos no habían atraído tanto la atención como el Sovaldi. Las ventas de Sovaldi llegaron a 10.283 millones de $ en 2014. El laboratorio multiplicó por cuatro sus beneficios entre 2013 y 2014 (Bañuelos J 2015). Y, al mismo tiempo, en España y en otros países de la UE miles de pacientes no pudieron acceder a los tratamientos en 2014, y están teniendo dificultades para acceder en 2015.
Es la primera vez que en los países llamados “desarrollados” o de ingresos altos, como España, se tiene que racionar un medicamento. Es decir, hay pacientes que podrían haber mejorado su salud o incluso evitado su muerte prematura, que no han podido tomar esta medicina porque el laboratorio ha pedido precios muy altos y las negociaciones con las autoridades sanitarias de los países han retrasado la incorporación del medicamento, estableciendo finalmente criterios de autorización restrictivos y/o mecanismos de aplicación limitados.
En la Unión Europea viven entre 7,3 y 8,8 millones de personas con el virus de la Hepatitis C. Varios miles de personas mueren cada año de forma prematura. Es una epidemia de enorme proporción y gravedad (EASL 2014). Es importante señalar que estos medicamentos deberán confirmar su seguridad y eficacia de los efectos terapéuticos en el medio y largo plazo. Pero, hasta el momento, los datos muestran unos buenos resultados.
La Constitución de la Organización Mundial de la Salud, la Declaración de los derechos humanos, el Pacto Internacional sobre los Derechos Económicos, Sociales y Culturales, y la Constitución española protegen el derecho a la vida y a la protección de la salud. “Disfrutar del estándar más alto de salud que se pueda conseguir, es un derecho fundamental de todo ser humano, sin distinción de raza, religión, orientación política, o condición económica y social” (WHO 1946). El acceso a las medicinas esenciales es una dimensión del derecho a la salud que se puede y se debe conseguir.
Hoy en la UE ese acceso no está siendo garantizado, y para garantizarlo debería realizar unos desembolsos tan elevados que pondrían en dificultades a los sistemas de salud, o impedirían atender otros problemas de forma adecuada. Las asociaciones de pacientes, como la Plataforma de afectados por Hepatitis C en España, han realizado acciones de protesta (manifestaciones y encierros) y han presentando sus demandas ante los Gobiernos, los Tribunales de Justicia y el Parlamento Europeo (PlafHc 2015).
En Portugal un grupo de pacientes de Hepatitis C llevó su protesta ante el Parlamento y ante el Ministerio de Sanidad. El conocimiento a través de los medios de comunicación de la muerte de un paciente esperando el tratamiento, y distintas intervenciones en el Parlamento crearon suficiente presión política sobre el gobierno y las compañías farmacéuticas, forzando un acuerdo que, en principio, asegurara el acceso de los pacientes a los nuevos tratamientos de acuerdo con los criterios y prioridades clínicas.
Estas tensiones, y el problema de fondo que supone la barrera de acceso por el alto precio han sido recogidos por distintas organizaciones intergubernamentales y no gubernamentales y por organizaciones de profesionales sanitarios, como la OMS, Cruz Roja, Médicos del Mundo o Médicos sin Fronteras.
La Organización Médica Colegial de España señaló en enero de este año (OMC 2015-1) que “en la incorporación de fármacos innovadores de eficacia y seguridad demostrada debe primar antes la salud pública y el interés de la atención sanitaria a los pacientes; y que el beneficio industrial debe ser prudente y proporcionado a los costes de producción e investigación, estableciendo un precio justo negociado”.
La Comisión Europea ha planteado la posibilidad de utilizar el mecanismo de compra conjunta voluntaria de varios países miembros. En marzo de este año la Oficina Regional Europea de la OMS ha publicado un informe muy completo sobre el acceso a los nuevos medicamentos, incluyendo la discusión sobre el problema de los precios (WHO 2015-2).
También la Asamblea Mundial de la OMS ha acordado en mayo de este año una Resolución para que todos puedan acceder a vacunas a precios accesibles. La resolución urge a los Estados Miembros a aumentar la transparencia en la fijación de los precios de las vacunas y explorar la posibilidad de hacer compras conjuntas (WHA 2015).
El asunto de la fijación de precios de los medicamentos, y de cómo se financia la investigación y el desarrollo de los mismos, merece reflexión y debate para intentar llegar a un equilibrio que garantice los derechos de la persona y tenga en cuenta los intereses de todas las partes.
2.
¿Cómo se calculan los precios? Como ya hizo ver Margaret Chan, Directora General de la OMS, “las discusiones [sobre acceso a medicinas] casi inevitablemente giran hacia cuestiones de precios, patentes, protección de la propiedad intelectual y competencia” (WHO, WTO, WIPO 2013).
Todos tenemos experiencia de comprar o vender cosas. Pero ¿cómo se fijan los precios? El precio es la cantidad de bienes o servicios que alguien quiere obtener a cambio de su producto. Esa cantidad puede traducirse en moneda, entonces el precio es la cantidad de dinero que alguien pide a cambio de su producto (Lamata 1994).
La persona que adquiere el producto obtiene un valor (resuelve un problema, satisface una necesidad). El valor del producto para el que lo adquiere es mayor que para el que lo produce. El precio divide este valor entre los dos lados de la transacción (Pita 2014).
Hay dos formas de fijar los precios de un bien o servicio: por su COSTE (lo mínimo que el fabricante necesita para seguir fabricando), o por el VALOR (lo máximo que el consumidor está dispuesto a pagar por el valor o beneficio que espera obtener).
En un sistema de libre mercado y libre competencia, cuando una empresa fija el precio de un nuevo producto por el “valor” de la satisfacción que logra en el cliente, tiende a poner el precio más alto que el cliente está dispuesto a pagar y puede pagar, porque en ese momento el producto es único y se supone que es mejor que los anteriores. Pero inmediatamente surgen otros productos similares (en el caso de los medicamentos serían los genéricos y los biosimilares) que hacen lo mismo a menor precio, compiten por el cliente, con lo que obligan a bajar los precios, acercándose al precio de coste de producción. Para que la empresa no pierda dinero, el precio unitario por el número de ventas (consumo) deberá cubrir el coste marginal de producción (los costes de operaciones más el coste de oportunidad del capital invertido en la empresa). Si hay costes de I + D (que se transforman en costes fijos en el momento de producir el medicamento) entonces se debe encontrar un mecanismo para pagar por esa I + D, de forma que se incentive la innovación. El incremento de los precios es la opción más común, pero no tiene que ser necesariamente esta fórmula, como se discutirá más adelante. El mercado y la competencia ajustan la demanda y la oferta con los precios más convenientes para ambas partes.
En algunos mercados, puede mantenerse un equilibrio a lo largo del tiempo con productos de diferentes calidades a diferentes precios (los fabricantes de automóviles ofrecen variedad de coches con diferentes calidades a diferentes precios; se introducen innovaciones y se modifican los precios, sin que haya discusión sobre problemas de acceso a los productos). En muchos productos (bienes y servicios) puede haber variedades o calidades distintas con el mismo precio o precio similar (por ejemplo los libros o las películas). En ninguno de estos mercados hay un precio igual al “valor” más alto para los consumidores (ni siquiera a la media de la valoración) que sea fijado legalmente. Como se discutirá más adelante, el marco institucional creado para el sector farmacéutico contribuye a los problemas de precio y acceso observados.
En el caso de la salud, el “valor” de medicamentos que salvan vidas, es muy alto, por lo que el fabricante puede pedir un alto precio, el precio máximo posible, aquél que haya alguien dispuesto a pagar. En principio fijará el precio de salida en EEUU, un país de renta alta donde hay personas que pueden pagar, y donde las empresas farmacéuticas fijan el precio que consideran conveniente, porque el sistema sanitario público (Medicare) tiene prohibido por ley negociar precios. Se fija, pues, el precio más alto posible. A partir de ahí, la industria tratará de imponer el precio a los demás países. Pero ¿no actuará entonces la competencia bajando los precios? Pues no. En el caso de los nuevos medicamentos no es así, porque las empresas han logrado, en las últimas décadas del pasado siglo, que los gobiernos “interfieran en el mercado” prohibiendo la competencia durante un tiempo determinado mediante el sistema de patentes (que analizaremos en la Sección 5). De esta forma la empresa ejerce el llamado “poder de mercado”, monopolio sin competencia. Entonces las empresas calculan cuánto es lo máximo que puede pagar (el paciente, o el país); hacen un estudio de la capacidad económica, la renta disponible, y lo que podrían conseguir; y fijan el precio más alto posible.
Pero ¿cuál es la razón que justifica que los gobiernos concedan las patentes? Las patentes tienen como justificación remunerar el coste de la inversión en investigación para estimular y garantizar la innovación. Por lo tanto, si se concede patente para proteger la inversión, entonces se debe fijar un precio según los costes de producción, incluyendo la I + D (costes debidamente auditados, para evitar la imputación de costes injustificados o innecesarios) y un beneficio razonable, no abusivo. Por el contrario, si se deja que una empresa ponga el precio de un producto por su “valor”, el máximo precio posible, entonces no se debería conceder una patente que impida la competencia, o se debería retirar una vez concedida.
En la literatura económica es bien conocido que las patentes no conducen a la asignación más social de los recursos. Las patentes son vistas como un “coste” (precios más altos, por encima del coste de producción), para obtener un “beneficio” (una tasa de innovación más alta). La cuestión es, por una parte, si el balance actual entre “coste” y “beneficio” del sistema de patentes es adecuado y, por otra parte, si podemos encontrar y usar otros mecanismos para compensar la innovación y poder ofrecer a los pacientes un acceso mejor a los nuevos medicamentos.
Debemos tener en cuenta otro factor importante en los equilibrios para fijar los precios. Cuando los pacientes están cubiertos por un sistema nacional de salud, o por un sistema público de seguro sanitario, no tienen que pagar los medicamentos en el momento del uso (en los casos, por supuesto, de que esté aprobada la financiación pública de los mismos). En esta circunstancia los pacientes tienden a centrarse en el acceso independientemente de los precios, lo que genera una presión añadida sobre los gobiernos y las compañías de seguros (dependiendo de los países).
LAS CONTRADICCIONES DEL PRESIDENTE OBAMA En Ia propuesta de Presupuesto para 2016 presentada por el Presidente Obama en el Congreso de los EEUU, hay dos asuntos importantes. Por un lado pideal Congreso que autorice a Medicare Ia posibilidad de negociaciar los precios de los medicamentos con Ia industria farmaceutica, una facultad que esta prohibida explicitamente porIa legislaci6n actual. Por otro lado, propone que se dote una partida de 215 milIones de d61ares para Ia "lniciativa de Medicina de Precision", o medicina personalizada, para explorar las bases moleculares y geneticas de las enfermedades creando una cohorte de mas de un mill6n de personas voluntarias para investigaci6n y reforzando varios lnstitutos y programas de investigaci6n nacionales. Robert Pear, articulista de New York Times (Pear R 2015), veia una contradiccion entre estas dos propuestas, ya que Ia segunda va dirigida a desarrollar nuevas medicinas que son de altisimo precio, mientras que Ia primera intenta controlar y reducir el crecimiento de los precios de los medicamentos.
Sin embargo no hay contradicci6n aqui. La contradicci6n esta en que, recibiendo Ia investigaci6n una importante financiaci6n publica (50% del total), Ia industria pueda utilizar como argumento el alto coste de Ia investigaci6n paraJUStificar altisimos precios Medicare deberia negociar los precios en funci6n de los costes de Ia fabricaci6n, incluyendo los costes reales de I+D aportados con fondos privados (descontando Ia financiaci6n publica). Entonces los precios serian mucho mas bajos que los actuales (que superan muchas veces los 100 000 dolares por tratamiento y ario). Otra alternativa seria que toda Ia investigaci6n para los medicamentos se hiciera con fondos publicos, a traves de Agencias lnternacionales financiadas por los paises (OMS) y que los precios de los medicamentos solamente se basaran en coste de producci6n, sin protecci6n de patente Asise resolveria Ia contradicci6n.
- ¿Cuál es el coste, cuál es el precio y cuál sería un precio razonable de un medicamento innovador? La aparición de los nuevos medicamentos para tratar la Hepatitis C, que podrían beneficiar a un número muy elevado de pacientes, y el elevado precio que han fijado las empresas farmacéuticas, ha motivado el debate y la reflexión de numerosos autores sobre la necesidad de buscar un sistema de fijación de precios más razonable, más justo. Así lo plantea, por ejemplo, Martínez Olmos (2015): “...es muy necesario y conveniente propiciar un sistema de fijación de precios en los medicamentos que ofrezca total transparencia a la sociedad sobre los costes reales que se hayan invertido en investigación y producción de las nuevas terapias para justificar el precio de las mismas…”.
Analicemos el ejemplo que nos ocupa: ¿Cuál es el coste de fabricación del sofosbuvir? Un primer problema con el que nos encontramos es no disponer de información detallada de los costes de los medicamentos, que deberían ser publicados por los laboratorios y validados por fuentes independientes (no financiadas por los laboratorios) que los hubieran auditado. Esta es una información que parece exigible cuando se trata de fondos públicos. ¿Aceparíamos que se compraran equipamientos o se contratara la construcción de un edificio público sin que la sociedad pudiera saber los costes? ¿Cómo fijar, entonces, el precio de salida del concurso público? ¿Cómo saber si lo precios que se ofrecen son razonables, o si proponen bajas temerarias? Todas las compras públicas tienen que justificarse con cuentas transparentes para garantizar que se utiliza el dinero público de la manera más eficiente. En este caso no parece que sea así, por lo que tenemos que basarnos, mientras tanto, en estimaciones.
En el estudio de Andrew Hill y colaboradores (Hill A et all 2014), de la Liverpool University, se estima que el coste de producción para un tratamiento de 12 semanas con sofosbuvir es inferior a 110 euros. Si a ese coste le añadiéramos una estimación del coste de la investigación, aplicando el porcentaje que dedican las empresas farmacéuticas a esta actividad en relación con el que dedican a la fabricación, (Pharmaceutical Sector Inquiry EC 2009), podríamos añadir otros 80 euros por tratamiento. Si añadimos un coste de marketing de 60-110 euros por tratamiento el coste por tratamiento de 12 semanas de sofosbuvir ascendería a 250-300 euros.
Otra estimación de los costes de fabricación es a partir de los precios de los genéricos que se han aprobado en la India, fabricados por varias compañías como Natco Pharma (Dna 2015) o Hetero. El precio para un envase de 28 tabletas de 400 mg es de 19.900 Rupias, o 297 euros. Estos precios no incorporan el coste de la investigación, que podemos estimar en 80 euros por tratamiento, pero sí incorporan un porcentaje de beneficio y otro porcentaje que deben pagar a la propietaria de la patente, que serían, al menos, una cantidad equivalente.
¿Cuál es el precio del sofosbuvir en España? De manera sorprendente e injustificable también aquí nos encontramos con un problema de falta de información. No se ha publicado el precio al que la empresa está facturando a los diferentes países o seguros de salud. Se comenzó hablando de 74.000 euros en EEUU, aunque luego se supo que en aquél país, y en los demás países, la compañía farmacéutica cobra diferentes precios a diferentes clientes, aunque no los hace públicos.
En España el Ministerio de Sanidad tampoco ha hecho públicos los precios que ha establecido para los nuevos antivirales. En una nota de prensa del 26/2/2015 (MSSSI 2015) informaba que “en la negociación se han empleado fórmulas de “riesgo compartido”, una “tarifa plana” (significa que el SNS paga lo mismo si el tratamiento dura las12 semanas establecidas que si hay que ampliarlo a las 24 semanas), el “precio por volumen” (a más pacientes baja el precio) y el “techo de gasto”. En concreto, se ha establecido un techo de gasto de 727 millones de euros, a pagar en tres años…”.
En la misma nota se decía que, de acuerdo con los criterios del grupo de expertos redactor de la propuesta de Plan Estratégico Nacional para el abordaje de la Hepatitis C, y teniendo en cuenta los datos de las CCAA, el número de pacientes a tratar es 52.964, de un total de 95.524 pacientes diagnosticados. Aunque conviene recordar que en España se estima que viven con el virus de la Hepatitis C entre 700.000 y 900.000 personas.
Con esta información podríamos deducir aplicando una sencilla división que el Ministerio ha aceptado un precio por tratamiento de 13.990 euros. Podemos suponer que se incluye en ese precio una media de dos tratamientos con antivirales de nueva generación. Entonces, el precio de un tratamiento con un nuevo antiviral como el sofosbuvir, ascendería a 7.500 euros. Si el coste, como se ha visto antes, fuera de 300 euros por tratamiento, resulta una cantidad extremadamente alta y desproporcionada: 25 veces lo que cuesta, es decir, un 2.500 % más (incluyendo el pago de los costes de I+D).
Pero probablemente, según la información disponible de los propios hepatólogos, el precio del tratamiento combinado se sitúa entre los 20.000 y los 30.000 euros dependiendo de la combinación utilizada pare el tratamiento de 12 semanas. Con lo cual, las cifras serían aún más desproporcionadas (67 veces lo que cuesta, un 6.600% más). En este mismo sentido, el Gobierno Vasco ha publicado que el gasto para los nuevos tratamientos entre enero y el 12 de mayo de 2015 ha ascendido a 41.000 euros por paciente (Lago C 2015).
La propuesta de Plan Estratégico elaborada por el grupo de expertos contiene elementos positivos, aunque carece de un elemento fundamental, la discusión sobre los recursos necesarios (tanto para financiar los medicamentos, como para facilitar el diagnóstico y seguimiento de los tratamientos en los centros sanitarios, lo cual retrasará en la práctica la atención a los pacientes). Por otro lado, la negociación a que se hace referencia para fijar los precios (suponemos que entre el Ministerio de Sanidad y las empresas farmacéuticas) no ha logrado acordar un precio justo. Aparentemente logra un buen resultado, porque el precio inicial que pedían las empresas farmacéuticas era mucho mayor. Pero el problema es que se discute a partir de un precio artificialmente muy alto y sobre ese precio se fija una “rebaja”, “tarifas planas”, “costes compartidos”, etc., dando la impresión de que la empresa hace un favor al Ministerio y a los pacientes, cuando no es así. El precio que, al parecer, se habría acordado, seguiría siendo entre 25 y 50 veces el coste de producción. Es decir, el sistema público de salud gastaría entre 700 y 1.400 millones de euros más de lo necesario; esos recursos se detraerán de otras necesidades de atención, del gasto en otros medicamentos o en otro tipo de servicios, o se añadirán al déficit de las cuentas públicas, debilitando el sistema de salud (y esto solamente para le tratamiento de una enfermedad, y para los pacientes que ya están diagnosticados, que son solamente una parte de los que deberían recibir el tratamiento). La negociación de precios debe partir del coste de producción, incluyendo los costes de la investigación y el desarrollo del producto, debidamente auditados. Aunque se compense a los accionistas de manera generosa por la investigación y el desarrollo de nuevos medicamentos, estamos muy por encima de un retorno justo para la innovación.
Tampoco es correcta la decisión del Ministerio de Sanidad de incorporar un nuevo medicamento, con un impacto presupuestario importante, sin acordar el aumento de la financiación a las CCAA. Se acuerda, en cambio, la posibilidad de acceder a préstamos y, además, se hace en forma finalista (creando un “silo”) para este grupo de tratamientos, lo cual es un mal precedente a la hora de abordar la financiación del conjunto de los servicios sanitarios públicos.
En todo caso, cabe insistir también aquí en la necesidad de transparencia en la información sobre costes y precios de los medicamentos, para poder contestar a la siguiente pregunta relativa a si los precios son exagerados y abusivos o son razonables. Por eso debe exigirse el cumplimiento de la Ley de Transparencia, acceso a la Información Pública y Buen Gobierno. En este sentido la Comisión Nacional de los Mercados y la Competencia llama la atención sobre la no publicación de informes motivados de resolución de financiación y precios (CNMC 2015).
¿Cuál sería el precio razonable de estos medicamentos? El concepto de “razonable” o “abusivo” es relativo. Supongamos que el alquiler mensual de un piso costara 1.000 euros, ¿estaríamos dispuestos a pagar 25.000 ó 50.000 euros por ese alquiler mensual? Seguramente estaremos de acuerdo en que no sería razonable que nos pidieran esa cantidad. Sería un abuso y, si no tuviéramos otra alternativa para alojar a nuestra familia, lo calificaríamos de robo y nos tendríamos que quedar a la intemperie.
A la vista de los datos revisados hasta este momento, ¿Se puede afirmar que se ha producido un uso abusivo de las patentes en España? Partimos del hecho, no justificado, de no conocer los costes detallados y desglosados de este nuevo medicamento (el escandallo).
Partimos de otro hecho, tampoco justificado, de no conocer el contenido de los acuerdos con la industria y el precio final establecido.
El precio justo debe cubrir el coste de producción. En el caso de que el producto incorpore investigación y desarrollo, el precio debe fijarse buscando la remuneración que cubra la inversión realizada en I+D y permita, además, obtener un beneficio razonable. Ya hemos visto que con 300 euros por tratamiento se cubren los costes de producción e investigación. Hemos de ponernos de acuerdo en cuál es el beneficio razonable. El Ministerio de Fomento calcula un 6% de beneficio industrial en sus licitaciones. Parece que un beneficio de entre un 6 y un 10% podría ser razonable.
Llegaríamos a un precio razonable de 330 euros por tratamiento.
Con la información disponible, que se ha comentado más arriba, si el precio que se ha aprobado para un medicamento fuera 20 veces su coste, o más, podríamos afirmar que se trata de un precio exagerado, abusivo. Todo lo que exceda un 10% de beneficio, bajo protección de patente, sería excesivo.
La fijación de estos precios tan altos se puede hacer porque el medicamento está protegido por el uso de la patente (cuando se autorizan y fabrican genéricos, los precios bajan en una proporción importante). Entonces se puede calificar la situación como uso abusivo de la patente.
Con este mismo método de fijación y negociación de precios para otro tipo de medicamentos y otro tipo de enfermedades, el resultado es similar. El problema del método de fijación de precios para los nuevos medicamentos es un problema de gran dimensión para el presente y el futuro de los sistemas sanitarios en España, en Europa y en el Mundo que pone en riesgo la viabilidad de dichos sistemas.
Como señaló Jeffrey Sachs al comentar el caso de Sovaldi: “El desafío … es adoptar un sistema racional de precios para los medicamentos que continúe impulsando descubrimientos científicos excelentes al mismo tiempo que mantenga la codicia bajo control” (Sachs J 2015).
Como veremos después, incluso en los EEUU, un país que tiene tradición de libertad en la fijación de precios, hay protestas en relación con los altos precios de los nuevos tratamientos para la Hepatitis C, y una compañía aseguradora ha iniciado un procedimiento ante los tribunales contra la compañía farmacéutica por los precios abusivos.
Las compañías negocian precios en ámbito nacional teniendo en mente cómo puede afectar el precio fijado en un país sobre los precios que se fijarán en otros países. De esta forma rechazarán acuerdos de precios más bajos, para evitar la aplicación automática mediante el sistema de precios de referencia en otro país. La discriminación de precios (sobre una base de precios “justos”) entre diferentes países, basada en diferentes factores, como la capacidad de pago, podría tener un efecto positivo en el resultado global en términos de bienestar. Pero puede tener también efectos negativos al imponer precios exagerados en países de renta media y alta, y precios demasiado altos en países de renta baja, afectando a la población de todos los niveles de ingreso.
4.
La espiral de precios de los nuevos medicamentos. El ejemplo de los medicamentos oncológicos.
En septiembre de 2012 el Sloan Kettering, uno de los hospitales más importantes de los EEUU dedicados al cáncer, rechazó por primera vez en su historia la incorporación de un tratamiento (Zaltrap). Cuando le preguntaron al Dr Saltz, presidente del comité de farmacia del hospital, la causa de la no inclusión, contestó: “a causa del precio” (NYT 2013).
En los países en desarrollo, es decir los países de bajos ingresos, siempre ha habido problemas de acceso a los medicamentos por causa de su precio. Esto se ha denunciado por diversas organizaciones (OMS, Médicos del Mundo, Médicos sin Fronteras, Cruz Roja, etc.) y en diversas ocasiones se han llevado a cabo iniciativas, desde los países de ingresos altos, para paliar esa situación (ayuda humanitaria, cooperación, etc.). Sin embargo, en los países de ingresos altos no se había planteado el problema de falta de acceso a los medicamentos por el problema del precio. Hasta ahora. Hasta que, desde hace diez años las empresas farmacéuticas han iniciado una espiral acelerada de precios para los nuevos medicamentos llegando a un nivel que tampoco los países de ingresos altos pueden pagar.
El Dr Kantarjian, oncólogo estadounidense, viene llamando la atención sobre esta cuestión al ver que muchos pacientes con cáncer no podían acceder al tratamiento por el elevadísimo precio de los nuevos medicamentos (Kantardjian H et al 2014). Su última iniciativa es promover una petición pública al Congreso de los Estados Unidos para que se modifiquen los precios de los medicamentos y se hagan más accesibles (Silverman E, 2015): “Los precios están creciendo a niveles catastróficos”.
Afirma Kantarjian que “permitir que fije los precios un mercado dominado por el fabricante ha hecho que los precios de los medicamentos para el cáncer crezcan fuera de control”. Y se pregunta: “¿Puede aceptarse moralmente que se fijen precios tan elevados que, sumándolos, puedan llevar a la bancarrota al sistema sanitario, que no permitan a los pacientes acceder al tratamiento o les causen la bancarrota? (Kantarjian 2013-2).
Junto con otros colegas reflexionaba sobre las causas de los precios tan elevados de los nuevos medicamentos en EEUU, analizando en primer lugar los argumentos de los defensores de esta situación (Kantarjian et al 2014; Kantarjian 2013-2): -“Cuesta 1000 millones de dólares o más desarrollar un medicamento hasta poderlo introducir en el mercado”.
-“Los precios se basan en el beneficio o valor para los pacientes” -“Las fuerzas del libre mercado se encargan de que los precios alcancen niveles razonables”.
-“Si se controlan los precios o se reducen demasiado, se desincentiva la investigación para nuevos medicamentos”.
Estos argumentos, según el citado autor, no se sostienen. Para justificar su rechazo expone una serie bien elaborada de datos objetivos que resumimos por su importancia a continuación.
-El coste de la investigación y desarrollo de un nuevo fármaco está más cerca de los 100 millones de dólares que de los 1.000 que dice la industria. [Pero, aunque fueran 1.000 millones de dólares, este gasto es para todas las ventas del medicamento en todos los países donde se distribuye y no justifica precios tan elevados].
-Muchos medicamentos no tienen valor añadido, no generan beneficio significativo para el paciente y, sin embargo, una vez aprobados por la Agencia del Medicamento (FDA norteamericana) ponen un precio tan elevado o más que el último aprobado. [En este mismo sentido la revista Prescrire llamaba la atención sobre el hecho de que de 97 medicamentos nuevos, o con nuevas indicaciones, aprobados en 2010, únicamente 4 tenían ventajas terapéuticas (Prescrire Int 2011)].
-Las fuerzas del mercado no operan en este sector para bajar los precios. Se funciona en un régimen de monopolio, bien sea por la protección de la patente, o bien sea por acuerdos explícitos o tácitos entre las empresas. Medicamentos originales, con similar efecto terapéutico no bajan los precios, sino que los siguen subiendo. En muchos países las regulaciones de precios debilitan la competencia de precios que pudiera existir.
-No hay evidencia de que los precios más bajos reduzcan la investigación. Muchos investigadores y profesionales sanitarios están motivados por razones humanitarias y científicas más que por las razones económicas. No están estimulados por altos salarios o bonos, como los directivos y altos ejecutivos de las compañías farmacéuticas. Gran parte de la I + D está pagada directamente con fondos públicos.
Además Kantarjian señala otras razones que contribuyen a que los precios sean tan altos en los EEUU: -La prohibición a Medicare para negociar precios con las compañías farmacéuticas, por lo que deben aceptar el precio fijado por dichas compañías.
-No hay evaluación costo-efectividad a la hora de incorporación de un nuevo medicamento.
- Estrategias para retrasar la aprobación, producción y comercialización de los genéricos, que sí bajan los precios (“Pay-for-delay”).
- La prohibición de la importación de medicamentos para uso personal.
-La burocracia excesiva en la gestión de ensayos clínicos.
-Los intermediarios: organizaciones de gestión de contratos de investigación y gabinetes de abogados.
-Los gastos de “formación” de los médicos (congresos, reuniones, consejos asesores, etc.) -La aceptación tácita de los médicos.
-La sobrevaloración de pequeñas innovaciones por los expertos y las sociedades científicas -La resistencia de las asociaciones de profesionales y de pacientes a exigir la evaluación costo-efectividad, por el miedo a la pérdida de apoyo de la industria.
-Los excesivos costes por la distribución, mayorista y minorista.
Las soluciones que propone el autor reseñado para controlar esta espiral en el crecimiento de los precios son las siguientes:
- Fijar un precio razonable, que permita obtener a las compañías un beneficio justo.
- Reducir los costes de la investigación: burocracia en los ensayos clínicos; intermediarios; distribución, etc. [Para que esta medida de reducción de costes fuera eficaz debería asegurarse que se tradujera en una reducción de los precios; si los precios se fijaran por valor, la reducción de costes beneficiaría a las empresas solamente].
- Utilizar la valoración de la efectividad de un nuevo medicamento para que los seguros de salud, los hospitales, etc., lo incluyan o excluyan de su oferta terapéutica.
- Conseguir el apoyo de profesionales, asociaciones de pacientes, sociedades científicas, etc., para no crear expectativas exageradas sobre medicamentos que no aportan valor, evitando la presión sobre su inclusión y su prescripción.
- Permitir a Medicare negociar los precios con las farmacéuticas, para bajar los precios.
- Eliminar las estrategias que retrasan la incorporación de genéricos. [Se refiere aquí a cuando han caducado las patentes, pero no analiza el tema de las patentes en sí mismo, y la relación con la fijación de precios, que para nosotros es clave].
- En el mismo sentido, permitir la importación de medicamentos originales o genéricos con menores precios.
Finalmente, otra de las propuestas que formula el autor es relacionar el precio con el valor, con el beneficio para los pacientes (medido, por ejemplo, en años de vida ajustados por calidad). Su propuesta intenta evitar que entren en el arsenal terapéutico medicamentos que no generan beneficio para el paciente, con un precio igual de elevado que los que sí que generan beneficio real, especialmente en el caso del cáncer, lo cual es positivo. Pero, en cambio, la fijación de precios por el valor, tiene problemas. Algunos países europeos están tratando de aplicar este enfoque, pero el resultado para los pacientes y los sistemas de salud no es favorable y puede tener efectos contrarios al deseado, como veremos más adelante.
El enfoque de análisis costo-beneficio es bueno para aceptar o no un medicamento en la financiación pública, pero no para la fijación de precio (al menos en ausencia de competencia, es decir, bajo protección de patente o similar, en cuyo caso, no hay presión para la bajada de precios, por lo que se debe optar por el cálculo de los costes y la fijación de precio sobre costes más un beneficio industrial razonable).
De alguna manera Kantardjian reconoce implícitamente que el argumento de fijar el precio por el “valor” no es el más conveniente para el paciente y la sociedad, ya que aboga por introducir cuanto antes los genéricos, a menor precio (porque la competencia tendería a bajar el precio acercándolo al coste de producción), es decir, por debajo del “precio por valor” del medicamento.
“Los retrasos en la introducción de genéricos, a través de estrategias de pagar por retrasar (pay-for-delay) o con genéricos de la propia compañía originaria, pueden dañar a los pacientes con Leucemia Mieloide Crónica y deben ser evitadas a toda costa” (Kantarjian 2013-1). Utiliza, entre otros, el ejemplo del imatinib, con un precio de 92.000$ por año de tratamiento. Los genéricos pueden tener un precio de 2 a 10.000€. En cambio, los nuevos medicamentos de marca, de efecto similar, costarán 100.000$ por año. Su propuesta es que la terapia inicial para los pacientes sea con el genérico de imatinib y que solamente se usen los nuevos de marca en los casos en que la anterior no sea eficaz.
Esta misma idea es expuesta por Santoro et al (2013), en respuesta a una propuesta de otros autores (Jabbour et al) que proponían usar la segunda y tercera generación de los inhibidores de la tirosina quinasa sin que se hubiera demostrado mayor tasa de supervivencia. Si el criterio utilizado para fijar el precio fuera retribuir por “valor”, el precio del genérico sería igual que el del medicamento originario, porque tienen el mismo efecto, el mismo “valor”. En el genérico se entiende que se fijará un precio cercano al coste de producción. En el medicamento originario se acepta un precio mayor, para cubrir el coste de la investigación realizada, pero no para fijar precios especulativos por el monopolio que concede la patente. En conclusión: no se debe aceptar fijar precio por “valor” (el máximo posible) si se tiene protección de patente.
Hay un uso abusivo de la noción de reflejar el valor en el precio. Una cosa es decir que el mayor valor de una innovación tiene que ser compensada en el precio. Otra cosa totalmente distinta es decir que los precios deben permitir a las empresas capturar todo el valor de la innovación que aportan al mercado.
En una economía que funcione bien los precios deben reflejar los costes de oportunidad de la producción. Un producto que tenga más valor para los consumidores pero que tenga un coste de producción menor, si hay competencia, tendrá un precio menor (aunque tenga un valor más alto por unidad consumida que otro producto con menos valor y costes de producción más altos). ¿Por qué, entonces, el argumento del valor? Este argumento, como estamos comentando, aparece en relación con la necesidad de compensar la I+D, con los incentivos para la innovación. Por un coste igual para I+D las compañías buscarán la innovación que les aporta más beneficios, que puede ser, o puede no ser, la que aporte más valor social. Fijar los precios según el valor genera el incentivo para desarrollar el producto que tiene más valor social. Sin embargo, esto solamente significa que se necesita crear un beneficio relativamente mayor para la empresa que desarrolla el producto con mayor valor social. Esto no significa que se fuercen los precios al máximo posible bajo la protección de la patente. Y esto también subraya que el problema de precios exageradamente altos tiene su raíz en la cuestión de cómo compensar la innovación. La solución, pues, tendrá que diseñarse también a este nivel.
5.
El sistema de patentes: Un breve análisis.
Con la patente se pretende compensar al inventor por el esfuerzo y el dinero invertidos en una creación de interés público. Con ello se intenta estimular el avance y la investigación científica y tecnológica del que se beneficia toda la sociedad (Sánchez Caro J, Abellán F, 2014).
Las patentes son uno de los instrumentos que la sociedad ha desarrollado, a través de las respectivas leyes, para proteger la propiedad industrial, que es una forma de propiedad intelectual (siendo la otra los derechos de autor). Con la patente el Estado concede derecho de propiedad al titular de la patente sobre la exclusividad temporal de la explotación del invento, sea este un producto o un procedimiento. El titular de la patente consigue así un beneficio que le compensa por la inversión en investigación, y la sociedad se garantiza la difusión del conocimiento necesario para el desarrollo y producción del invento (Costa G 2006).
La tensión derivada del sistema de patentes es muy conocida, máxime en lo referente a las patentes de medicamentos. Hay dos intereses potenciales en conflicto: La industria farmacéutica a la que resulta preciso proteger durante un cierto tiempo las inversiones en innovación e investigación de fármacos, que tienen un elevado coste económico y, por otra parte, el Estado, que tiene como misión asegurar el acceso universal a los medicamentos.
Lo expuesto se acrecienta cuando las patentes se refieren a medicamentos esenciales, en la medida en que el derecho a tener acceso a dichos medicamentos, que pueden salvar la vida o mejorar sustancialmente el estado de salud de millones de pacientes, colisiona en muchos escenarios con el derecho de las compañías a proteger mediante patentes las inversiones que dedicaron para su desarrollo, estableciéndose altos precios para su adquisición.
En resumen, cuestiones tan complejas como las que resultan de las patentes y su relación con la salud, suponen siempre un desafío, que no es otro que el de conciliar adecuadamente el interés público con los beneficios privados (Sánchez Caro J, Abellán F, 2014). El concepto de equilibrio o balance entre estos intereses es clave (Moital I, 2014; Scotchmer S 2006) A lo largo de la historia se ha discutido mucho la conveniencia o perjuicio de la concesión de patentes para los medicamentos. Muchos médicos y muchas personas han considerado que la finalidad del medicamento es la mejora de la salud de los pacientes y no debería restringirse su acceso con las patentes por el riesgo de limitación que podría suponer la barrera del precio (Gotzsche P 2014). En España, el Estatuto de la Propiedad Industrial de 1929 prohibía expresamente patentar productos farmacéuticos. Jonas Salk no quiso patentar la vacuna contra la polio. Ernst Chain y Howard Florey tampoco quisieron patentar el método para la producción industrial de la penicilina (Novoa 2014). Si lo hubieran hecho miles de personas no hubieran salvado la vida.
La patente para las moléculas farmacéuticas (patente de producto) fue incorporada hace relativamente poco tiempo en los países europeos: Alemania, 1967; Francia, 1968; Suiza, 1977; Italia, 1978. En España no se introducen hasta la ley de patentes de 1986, con entrada en vigor para los medicamentos el 7 de octubre de 1992, como consecuencia del tratado de Adhesión a las Comunidades Europeas (Lobo F 1989).
El derecho a tener acceso a los medicamentos, que pueden salvar la vida o mejorar sustancialmente el estado de salud de millones de pacientes, puede colisionar con el derecho de las compañías a proteger mediante patentes las fuentes de inversión que destinan a su desarrollo. ¿Se puede encontrar un balance adecuado? No solamente se puede, sino que se debe. Los derechos de propiedad intelectual e industrial son derechos creados socialmente y al servicio de valores que se aceptan por razones de utilidad, no constituyen un fin en sí mismo. Su finalidad es que la ciencia y la tecnología avancen.
“En esencia la naturaleza del problema reside en que la patente es un mecanismo que pretende generar el suficiente derecho de propiedad como para incentivar la innovación y el desarrollo tecnológico, pero no tanto como para que sea el poder de mercado asociado el que suponga una reducción del bienestar social” (Fanjul Martin O, 1983; citado por Lobo F 1989).
Por lo tanto, se debe lograr un equilibrio entre: -Por un lado, la protección de la inversión en investigación para fomentar el avance de nuevos medicamentos, asumiendo un mayor coste “actual” para la sociedad, al permitir a la empresa poner un precio más elevado, que incluye el coste de la fabricación y el coste de la investigación y desarrollo del nuevo producto, de manera que recupera su inversión obteniendo un beneficio razonable, -Y, por otro lado, el exceso de gasto para el paciente y para los sistemas públicos de salud, que puede suponer una barrera real para acceder a un medicamento que mejora la salud de los pacientes, en el caso de que los precios fijados sean abusivos.
Como hemos señalado, el sistema de patentes se desarrolló para poder proteger a las empresas innovadoras, y que éstas pudieran recuperar los costes de investigación, desarrollo y fabricación. La patente “interfiere” en el mercado y prohíbe copiar el producto original hasta pasados 20 años, de tal manera que la empresa pueda recuperar los costes y pueda seguir investigando.
El problema surge cuando se utiliza el mecanismo de patente (garantizar la recuperación de costes) y al mismo tiempo se fijan precios por “el valor”, por lo máximo que un paciente o un país está dispuesto a pagar, en una situación de monopolio (sin competencia, ya que está prohibida por la patente). Esto no es razonable. Es un abuso.
Es el caso que nos ocupa, con los exagerados precios fijados para los nuevos medicamentos. A esto se llama abuso de posición dominante en el mercado. La paradoja es que esa posición dominante y ese abuso lo ejerce la empresa, pero lo
generan (al conceder la patente) y toleran (al mantenerla) las propias Administraciones Públicas que son las que están obligadas a evitarlo.
Esta es la pregunta que deben responder los gobiernos de los países de la UE: ¿Debe proteger la patente la inversión en investigación, o el máximo beneficio posible que pueda alcanzar el propietario de la patente, poniendo los máximos precios que los clientes estén dispuestos a pagar y causando con ello perjuicio social, al evitar el acceso a las medicinas a miles de pacientes, o al exigir un desembolso injustificado a los servicios públicos de salud? El artículo 57 de la ley de Patentes española (Ley 11/1986, de 20 de marzo) señala que “la explotación del objeto de una patente no podrá llevarse a cabo en forma contraria a la Ley, la moral, el orden público o la salud pública”. En el Proyecto de Ley de Patentes que se está tramitando en el Congreso se mantiene esta limitación (art. 66) (BOC 2014).
El Comité sobre los derechos Económicos, Sociales y Culturales (CESCR 2005) deja bien claro que “en última instancia la propiedad intelectual es un producto social y tiene una función social”. Y añade que los Estados tienen el deber de prevenir elevados costes, no razonables, para acceder a medicinas esenciales… meditante la exclusión de la protección de la patente cuando se vea amenazada la realización plena de los derechos humanos.
Conflictos en relación con las patentes.
En EEUU se ha planteado un pleito ante el Tribunal de Distrito por la Autoridad de Transporte del Sudeste de Pensilvania contra la empresa Gilead, en relación con el medicamento Sovaldi, entendiendo que la explotación de la patente está “cargando precios exorbitantes” y que “los derechos del tenedor de la patente no deben traducirse en una licencia para ahogar con los precios los derechos de los pacientes y los programas de salud” (Chimicles NE et al 2014).
En la India y en Egipto las Oficinas de Patentes han rechazado alguna de las patentes relacionadas con sofosbuvir, por entender que no supone un nuevo descubrimiento, sino el uso de una molécula ya descubierta para otro fin (I-MAK 2015).
También Médicos del Mundo ha impugnado la patente de sofosbuvir, ante la Oficina Europea de Patentes, alegando que no supone una invención, ya que se basa en moléculas descubiertas previamente (MdM 2015).
Las empresas farmacéuticas tienen, a su vez, estrategias para mantener la vigencia de las patentes evitando así la competencia (fabricación de genéricos).
En la mayoría de los casos, las empresas protegen la explotación comercial de un producto con varias patentes relacionadas (a veces más de 1.000, en clusters de patentes) sobre diferentes moléculas, formas de uso, etc., de manera que pueden alargar la vigencia del monopolio.
En ocasiones, empresas originarias desarrollan sus propias empresas de medicamentos genéricos para acceder a nuevos mercados y controlar el uso de estos productos, reduciendo los beneficios de las empresas de genéricos y retrasando la entrada de dichos productos más baratos. Otras veces realizan adquisiciones de empresas de genéricos y bloquean así su desarrollo.
Como se puede comprobar, la utilización de las patentes no está exenta de conflictos (OECD 2014). La forma de aplicarlas es consecuencia de una relación de fuerzas. Un solo país, de tamaño y economía mediana, como España, tendría difícil fijar los precios en base a los costes. Un conjunto de países, como los que forman la Unión Europea, tendrían mucha mayor fuerza de negociación.
En todo caso, como ha señalado la Organización Médica Colegial (OMC 2015-2) “se debe revisar y reformar con urgencia el sistema de patentes” de tal manera “que el beneficio comercial no eclipse los verdaderos beneficios clínicos para los pacientes ni ponga en peligro la viabilidad económica de los sistemas nacionales de salud”.
¿Han servido las patentes para fomentar la investigación? Cuestión aparte, que también conviene tener en cuenta, es si realmente el sistema de patentes, el monopolio que otorgan, ha servido para lo que en teoría pretendía (por lo que obtiene justificación), es decir, la promoción de la investigación y la innovación, el desarrollo industrial y tecnológico. En un interesante estudio el profesor Félix Lobo concluía que el desarrollo de la industria farmacéutica en Alemania, Suiza, Reino Unido, Francia, Italia, Canadá y España no necesitó del sistema de patentes. Por el contrario, en algunos casos, la introducción de patentes fue contraproducente para el desarrollo de esta industria en los países (Lobo F, 1989).
Una reflexión similar, en relación con si los actuales incentivos para las empresas derivados de la protección de la patente y el poder de mercado para fijar altos precios promueven la investigación en nuevos medicamentos eficaces, podemos leerla en Light DW y Warburton R (2011). Según sus estimaciones el 85% de los nuevos medicamentos son muy poco o nada mejores que los anteriores.
Tampoco ha servido el sistema de patentes para promover la investigación de medicamentos dirigidos a tratar las enfermedades prevalentes en países de bajos ingresos que afectan a cientos de miles de personas y a decenas de países sin capacidad de pago, o para desarrollar medicamentos para enfermedades huérfanas. Es interesante, en este sentido, el análisis de Rens de Boer acerca del efecto que ha tenido la ampliación del tiempo de vida de las patentes a través del Certificado de Protección Suplementaria, CPS (Reglamento (EC) 469/2009), que puede conceder hasta 5 años más de protección a la empresa originaria. El autor constata que las patentes y los CPS estimulan la inversión hacia medicamentos valiosos económicamente, pero no hacia medicamentos valiosos terapéuticamente (de Boer 2015) Otra cuestión relevante es si podemos tener un sistema que funcione mejor que las patentes para recompensar y garantizar la investigación (Scotchmer S, 2006). Más abajo discutiremos este aspecto.
El “TTIP”: Un elemento nuevo que añade riesgo y genera intranquilidad.
El tratado para la Asociación Transatlántica de Comercio e Inversión (“Transatlantic Trade and Investment Partnership, o TTIP”) es un tratado que se está negociando en estos momentos entre la Unión Europea y EEUU que, según diversos analistas, podría poner en riesgo, entre otros derechos, la atención sanitaria pública.
Portavoces de la Comisión Europea y del Gobierno de los EEUU han destacado los objetivos declarados del acuerdo: disminuir las barreras al comercio de bienes y servicios, aumentar la actividad económica, crear empleo, disminuir costes, etc.
Llama la atención que teniendo objetivos aparentemente tan positivos las negociaciones sean secretas. Esta opacidad, y los antecedentes de otros tratados similares, explican que para muchos analistas el tratado pueda suponer justo lo contrario, pérdida de empleo, destrucción de empresas y un importante retroceso en derechos sociales.
Ante las críticas por la opacidad y la falta de información sobre las negociaciones, el 7 de enero 2015 la Comisión difundió información sobre el proceso de negociación TTIP.
En ella, en lo relativo al sector de los Servicios, la Comisión asegura que “la UE no adopta ningún compromiso en relación con los servicios de salud de financiación pública”.
Sin embargo, dada la naturaleza del Tratado y las obligaciones para los Estados Miembros, no es suficiente decir que no se incluyan apartados relativos a la sanidad o la salud pública. Es precisa una exclusión “explícita” de estas materias, para que no haya duda en la interpretación de otros artículos generales del acuerdo, cuyo contenido se podría querer ampliar a estas áreas.
En relación con la protección de la Propiedad Intelectual, patentes, etc., se dice que “no negociaremos normas de Propiedad Intelectual que cambien este delicado balance, o que pongan más presión en los presupuestos sanitarios públicos”. El problema es que el balance actual del sistema de patentes está poniendo ya mucha presión en los presupuestos sanitarios públicos. Es decir, el modelo actual no es adecuado, o no se está aplicando adecuadamente, y se debe cambiar.
En este caso ¿quiere decir que se van a “blindar” los actuales modelos y equilibrios de IP? Este blindaje perjudicaría a los ciudadanos. Es este modelo, precisamente, el que hay que revisar.
6.
La fijación de precios de los medicamentos en España En España el Gobierno tiene la competencia para decidir -la autorización para comercializar un medicamento -la inclusión de un medicamento en el Sistema Nacional de Salud y su financiación pública -la fijación del precio del medicamento.
Para decidir incluir un nuevo medicamento y financiarlo, se deben tener en cuenta una serie de criterios, como la gravedad de los procesos a tratar, su relación coste- efectividad, o la existencia de alternativas más convenientes. El RDL 16/2012 insiste en el criterio de coste-efectividad para la financiación selectiva.
Es decir, el estudio de coste-efectividad debería servir para decidir autorizar o no autorizar la financiación pública de un medicamento (y, quizá también, la propia autorización). Si lo que un medicamento aporta es menos efectivo (cura menos) a igual precio, o es más caro (con la misma efectividad), no se debería aprobar. Cosa distinta, como venimos señalando, y discutiremos en siguiente apartado, es que se usen los estudios de coste-efectividad para fijar los precios, posición que rechazamos, ya que puede suponer una mayor carga para los pacientes y la sociedad.
La Ley del Medicamento (29/2006, de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios) define una Comisión Interministerial de Precios de los Medicamentos, presidida por la persona titular de la Secretaría General de Sanidad y Consumo, y con un representante de cada uno de los ministerios de Economía, Hacienda e Industria, dos representantes de las CCAA y con el vicepresidente y el secretario del Ministerio de Sanidad.
Esta Comisión cuenta con un Comité Asesor de la financiación de la prestación farmacéutica del Sistema Nacional de Salud, compuesto por siete miembros, cuyos informes sirven para que la Comisión fije los precios.
Las personas que forman parte de la Comisión Interministerial de Precios de los Medicamentos y del Comité Asesor deberían estar sometidas a un estricto control de posibles conflictos de interés. Los requisitos para formar parte de estos órganos colegiados, el desempeño actual, y el régimen de incompatibilidades en el futuro (que impidieran tajantemente la “puerta giratoria”), deberían ser estrictamente regulados y supervisados por el Parlamento de la Nación y conocidos por la opinión pública.
Para fijar el precio del medicamento los laboratorios farmacéuticos deben presentar toda la documentación técnica, económica y financiera necesaria.
Tradicionalmente los precios se habían fijado teniendo en cuenta los costes de fabricación, y una estimación de los costes de investigación atribuibles al medicamento (el escandallo de costes); considerando además las posibles ventas (según los mercados donde se comercializa el producto), en función de las indicaciones autorizadas, se podía fijar un precio justo, que cubriera los costes más un margen de beneficio razonable.
Posteriormente se utilizaron precios de referencia. La financiación pública de medicamentos según los precios de referencia calcula el precio máximo a pagar por un medicamento incluido en un determinado conjunto, en relación con los productos de igual principio activo e idéntica vía de administración y menor precio (RDL 16/2012).
Al mismo tiempo, se comenzó a utilizar también una negociación con las empresas teniendo en cuenta el “valor” del medicamento, con diferentes aproximaciones (coste efectividad, coste beneficio, precio basado en el valor), partiendo del “dossier de valor” facilitado por las propias empresas que proponen el precio. Como señala con acierto Pere Ventayol parece que en esa cámara oscura en la que discuten los precios, al final éstos se fijan según la “capacidad que tenga el mercado de soportar ese precio” (Ventayol P 2015).
Analicemos con más detalle la cuestión de precio por valor, o por capacidad de pago.
7.
La fijación de precio a partir de una estimación del “valor”.
Hace 30 años, un ingeniero industrial experto en organizaciones y procesos de una empresa líder en informática, fue invitado por un grupo de industrias farmacéuticas a dar un seminario sobre control de calidad y costes. Al final de la jornada comentó con el responsable del seminario: “Me ha resultado llamativo que mientras explicaba el control de calidad, la trazabilidad de los productos, o la logística de la detección y respuesta a los fallos, han estado ustedes muy atentos y han hecho muchas preguntas; sin embargo, al hablar de costes casi no me han prestado atención y no me han preguntado nada”. Su interlocutor le contestó: “Es que nuestro problema en relación con los costes no es reducirlos, sino encontrar maneras de inflarlos para poder justificar precios más altos”.
El cálculo de precio por los costes no permitía fijar precios exageradamente elevados. En un primer momento se “inflaron” los costes de investigación. Pero como ese factor se puede objetivar y resolver con otras fórmulas de financiación, la industria viene defendiendo el cálculo de precio según el supuesto “valor” que aporta el nuevo medicamento, es decir, el precio más alto que puede pagar el cliente. Pero, al mismo tiempo, quiere mantener la protección de la patente, para evitar que la competencia baje los precios.
Este enfoque se plantea primero con un concepto atractivo: la importancia de valorar los resultados en salud y satisfacción obtenidos con una determinada atención sanitaria (outcome). Esto es importante. Se construye entonces el concepto de atención sanitaria basada en el valor (value-based health care), que tiene en cuenta la relación entre actividades sanitarias y resultados. Esta evaluación puede servir para orientar las actuaciones sanitarias, priorizar, incorporar o rechazar prestaciones, etc. Claro que hay que tener en cuenta los resultados, que son el objetivo deseado de las intervenciones sanitarias, pero cosa distinta es basar en ese concepto los modelos de pago, cómo se financian esas intervenciones, sus sistemas de remuneración, sus precios: poner el precio por “valor” (value-based pricing). Este cambio, sutil, es determinante.
¿Qué pasaría si utilizamos el mismo principio para calcular los impuestos sobre los beneficios de las empresas farmacéuticas: gravar sus beneficios hasta que se alcance el punto en que los accionistas logran los beneficios que obtendrían si invirtieran en una alternativa (digamos los beneficios medios de un “portfolio” en el mercado de valores)? ¿Value-based taxing?.
Un interesante artículo de la Unidad de Inteligencia de The Economist (commissioned by Gilead), plantea este enfoque como el modelo a seguir en Europa (The Economist 2015). Aquí aparece la confusión: si la medicina basada en el valor es “buena”, entonces el modelo de precio por valor es bueno, sin tener en cuenta que son cosas distintas, y que esos modelos de pago o financiación pueden ser menos eficientes y menos convenientes para los pacientes y los sistemas de salud. Sistemas con resultados en salud excelentes y muy eficientes pueden tener sistemas de pago tradicionales (por coste de los recursos empleados, complementados con incentivos variables en función de actividad y resultados). Sistemas que pagan por resultados pueden tener peores resultados en salud y ser muy poco eficientes. Son cuestiones diferentes.
Como punto de partida de la negociación de precio por valor (lo máximo que está dispuesto a pagar un cliente) se toma el precio fijado en EEUU (alta renta y prohibición de negociación del precio). Ese precio, fijado por el procedimiento del “valor”, empuja al alza. Por ejemplo, para el sofosbuvir el precio aceptado en EEUU era 74.000€. Después, se negociaban precios en Europa, en función de la renta del país, en Alemania 49.000€, en Reino Unido 44.000€, o en Francia 41.000€, aunque luego hay “descuentos” cuya cuantía no se ha hecho pública. Como el precio inicial en EEUU era mayor, da la impresión de que se obtienen precios ventajosos, cuando no es así.
El argumento de la industria es que se debe pagar por el “beneficio para el paciente”, calculando el beneficio en Años de Vida añadidos, en mejora de la calidad de vida, es decir años de vida ajustados por calidad (AVAC), o similar.
Este argumento se complementa con otro: pagar por el “ahorro”. Comparar el coste de ese nuevo medicamento y los AVAC conseguidos, con otros tratamientos alternativos usados previamente. Por ejemplo con el trasplante. ¿Cuánto está pagando el SNS por un trasplante de hígado? Pues eso es lo que VALE el nuevo medicamento. Pero no se tiene en cuenta que los costes de la realización de un trasplante son mayores y que son una última alternativa. Y, de nuevo aquí, se confunde la metodología para evaluar si un tratamiento es mejor, o no, que la alternativa, con el procedimiento para fijar el precio.
Al desligar el cálculo del precio de los costes de producción se pueden pedir unos precios tan altos como el cliente esté dispuesto a pagar. Con el criterio de coste- efectividad, los antibióticos, como la ampicilina, o algunos procedimientos como la apendicectomía, o la cura de una herida por una enfermera, o el diagnóstico de un profesional de atención primaria, aportarían muchos AVAC y podrían pedir precios de 25.000 euros o más por cada intervención. Un pediatra que diagnostique una neumonía en un bebé de un año y la trate con antibióticos de forma adecuada evitando la muerte prematura de la criatura, ha ganado 80 años de vida, con un coste total (consultas y medicamentos) de menos de 1.000€. Con un precio por AVAC de 37.500€, el precio de esta intervención sería 3.000.000€. Estos precios no se ponen a estos tratamientos, no porque no lo “valgan”, sino porque los precios en todos los demás factores de producción (personal, consumos, equipos médicos, construcción, etc.) se aceran a los costes. El argumento de precio por “valor, manteniendo al mismo tiempo la protección de patente” es insostenible.
Aunque este método de fijación de precios es menos favorable para los sistemas de salud, sin embargo diferentes foros académicos y políticos han ido introduciendo la recomendación de pagar por el sistema de “valor” en vez de por el sistema de “costes” (High Level Forum 2008; Kavanos P 2010; Rovira J 2012; WHO 2015). ¿Por qué? Pensamos que el objetivo de muchos autores al plantear este enfoque, como veíamos en el apartado 4 al comentar las propuestas de Kantarjian, es poder disminuir los precios elevados de nuevos productos que no aportan beneficios para el paciente. Esta situación es muy clara en el caso de medicamentos para el cáncer, donde nuevos fármacos que no aportan valor (por ejemplo, añaden un mes de vida sobre el medicamento anterior) se comercializan a precios muy altos (más de 100.000 dólares por tratamiento anual). Pero en estos casos, si el análisis de la efectividad (sobretodo en supervivencia) es negativo, lo que procedería es no financiar estos medicamentos con fondos públicos.
Otras razones que se argumentan para no utilizar el método de costes son la dificultad de auditar los costes, incluyendo los de I + D, la posibilidad de que se imputaran costes exagerados, o la posibilidad de que los costes fueran mayores de lo necesario por una gestión ineficiente. Estos problemas se pueden abordar desde los ámbitos nacionales o internacionales, de la misma manera que se abordan las compras de otros productos complejos, estudiando los costes al detalle o haciendo estimaciones en función de los datos disponibles.
En todo caso, teniendo en cuenta la aplicación que la industria está haciendo de la fijación de los precios por “valor” pidiendo precios muy por encima del coste, pensamos que el análisis coste-efectividad, es decir, el estudio de la efectividad de un medicamento o un tratamiento, y la puesta en relación con los costes de otros tratamientos vigentes, debería servir para incluir o no un medicamento o un tratamiento en el sistema de salud (o para retirar medicamentos ineficientes), pero no para fijar el precio. Son objetivos muy distintos.
Es decir, los estudios de coste-efectividad son útiles y deben usarse para no incluir, o excluir, medicamentos o prestaciones del SNS cuando no añaden valor, cuando no son efectivos. En este punto coinciden muchos expertos. Sin embargo, estos estudios no son la base más adecuada para la fijación de los precios. No es admisible fijar los precios según lo máximo que esté dispuesto a pagar (y pueda pagar) un paciente o un país (el valor) y al mismo tiempo limitar la competencia con la patente. No se deben usar los dos mecanismos a la vez. Como se ha dicho, la patente está pensada para recuperar los costes de I+D, no para subir el precio hasta lo máximo que alguien esté dispuesto a pagar (valor).
Algunos autores (van de Vooren K et al 2015) han analizado los estudios de evaluación económica publicados en relación con la Hepatitis C, señalando sus debilidades a la hora de tomarlos como base para la fijación de los precios. Ellos plantean que la fijación de precios en estos y otros casos similares no se puede basar en los análisis de costo- efectividad, sino que han de ir más allá. Señalan que es precisos discutir nuevas soluciones técnicas y proponen utilizar otros elementos de negociación del presupuesto, como precio por volumen en relación con los ahorros obtenidos por el tratamiento de los pacientes, o emplear otros mecanismos, como los concursos.
Estas estrategias de negociación de precios son interesantes, si fuera inevitable aceptar como punto de partida de la negociación los precios exageradamente elevados propuestos por las empresas (usando el criterio de “valor” y la protección de la patente). Se plantean entonces los “descuentos” o los mecanismos de “gasto máximo”, o “precio por volumen”, etc., que se negocian con los laboratorios farmacéuticos, tomando como referencia de partida la aprobación de precios exorbitantes en un determinado país. Así, en relación con esos precios tan elevados (más de 200 veces el precio de coste) se puede hacer un descuento importante, por ejemplo de la mitad, o incluso la décima parte del precio fijado inicialmente, y sigue siendo un precio elevadísimo (20 veces el precio de coste).
También se utiliza la estrategia de “riesgo compartido”, proponiendo al sistema de salud que pague siempre que el tratamiento logre una mejoría, pero dentro del marco de precios muy altos no justificados por el coste, con lo cual siempre se produce un gasto económico excesivo, no justificado y no sostenible, para el paciente o el sistema de salud. En todas estas estrategias, el punto débil de estos planteamientos es la aceptación inicial de negociar a partir de un precio injusto, muy por encima del valor de coste de producción (incluyendo I+D). Estos enfoques suelen ser propiciados por la industria.
En resumen, en el caso de los medicamentos y en ausencia de competencia, el precio debe fijarse esencialmente por el coste, debidamente auditado; el precio no puede ser fijado por el máximo que está dispuesto a pagar el paciente, o por el precio de otras alternativas igualmente necesarias pero que tienen más coste (por ejemplo, cirugía de trasplante).
8.
La financiación de la investigación.
¿Cuánto cuesta la investigación? Una de las razones que se aduce para no calcular los precios según los costes es que es que no se conocen los gastos de investigación imputables.
Y, al mismo tiempo, el principal argumento de la industria farmacéutica para que los gobiernos decidieran “proteger” las inversiones de la industria con patentes y otras ayudas públicas (desgravaciones fiscales, subvenciones, etc.) para “garantizar el descubrimiento de nuevos medicamentos”, es el supuesto altísimo coste de la investigación. Es decir, el argumento es “invisible”.
Hay muy pocas fuentes de datos disponibles para calcular los costes reales de la investigación. Los laboratorios farmacéuticos argumentan que esos costes son muy altos. Añaden que para que se obtenga una molécula eficaz, segura, se han investigado otras 10 donde no se han obtenido resultados. Esos costes deben cargarse en los precios de las moléculas de éxito. Bien, pero eso ¿cuánto cuesta? Siempre se podrá calcular el coste del salario de los investigadores, las instalaciones, las máquinas, los materiales de investigación, el capital invertido. La empresa tiene esos datos económicos y el Ministerio correspondiente tiene que tener acceso a los mismos, y se deben poder verificar, como cuando cualquiera de nosotros notifica unos gastos y unos ingresos. Se deben poder justificar.
La industria farmacéutica ha venido utilizando el estudio de DiMasi et al (2003) que concluía que los costes de I + D de un nuevo medicamento eran 800 millones de dólares. Si se proyectara hasta hoy serían más de 1.000 millones. El estudio se llevó a cabo en el Tufts Center for the Study of Drug Development (con importante financiación de la industria relacionada con la I+D de los medicamentos). El mismo autor y el mismo Centro actualizaron su estudio del coste de la investigación y desarrollo de un nuevo medicamento en 2014 (DiMasi 2014), situando dicho coste en 2.588 millones de dólares.
En línea con los trabajos de DiMasi, otros autores (Mestre-Ferrandiz et al 2012, de la Office for Health Economics, consultora entre cuyos clientes figura la industria farmacéutica) insistieron en el alto coste de la investigación (1.500 millones de dólares en precios de 2011). Este trabajo estaba financiado parcialmente por AstraZeneca y utilizó datos del Centre for Medicines Research International, CMRI, consultora propiedad de Thomson Reuters, que también asesora a la industria farmacéutica. Los datos económicos para los cálculos proceden de los estudios confidenciales facilitados por los grupos farmacéuticos. Es decir, este trabajo parece tener los mismos sesgos y conflictos de interés que el trabajo previo de DiMasi et al.
Sin embargo, Light y Warburton (2011), de las Universidades de Stanford y Victoria, criticaron la metodología del estudio de DiMasi (la obtención de la muestra, la falta de información sobre los datos enviados voluntariamente por las industrias que quisieron participar, la imputación de gastos financieros sobredimensionados, etc.) y concluyeron que, corrigiendo los sesgos, el coste de I + D de un nuevo medicamento era en 2003 de 43,4 millones de dólares, y hoy sería aproximadamente de 100-125 millones de dólares.
La Comisión Europea hizo un análisis del sector farmacéutico (EC 2009), estudiando datos de sus gastos entre 2000 a 2007. Según sus cálculos el gasto en investigación y desarrollo era un 17% del total, algo menor que los de fabricación, 21% y que los de marketing, 23%.
Los doctores Light y Kantarjian (2013) analizaron nuevamente esta cuestión, mostrando que el coste medio de la investigación de un nuevo medicamento (incluyendo los costes de oportunidad del capital invertido por la empresa y el coste de los medicamentos “fallidos”) se situaría en los 125 millones de dólares, es decir, 110 millones de euros.
Especial interés tiene la información facilitada por la “Drugs for Neglected Diseases initiative” que, basándose en su propia experiencia de 10 años de investigación y desarrollo de nuevos medicamentos, calcula el coste de I+D que han tenido para el desarrollo de un nuevo medicamento (incluyendo los medicamentos fallidos), y lo sitúan entre 100 y 150 millones de euros (DNDi 2014).
En todo caso, los laboratorios farmacéuticos deberían aportar y justificar la documentación sobre sus costes, incluidos los de I + D, junto a la propuesta de precios. En el ámbito de la Unión Europea se podría hacer una estimación más completa, para lo cual sería útil la creación de un Comité Parlamentario para el análisis de los precios de los nuevos medicamentos. Pocos asuntos son tan importantes para los ciudadanos europeos como el acceso a los servicios de salud y los medicamentos. El secretismo en una materia tan importante para la vida y la salud de las personas puede calificarse de secuestro de la democracia, ya que impide el acceso a una información necesaria para una asignación eficaz de los recursos públicos.
Por otra parte, en un informe de la OMS (WHO 2012) elaborado por un grupo de expertos sobre la coordinación y financiación de la Investigación y el Desarrollo en el sector sanitario, se dice cuando se estudió el gasto en investigación en todo el mundo para sanidad (en el año 1992), se encontró que del total de gasto (55.800 millones de dólares) el 50% era gasto público, el 49% privado y cerca del 1% de organizaciones sin ánimo de lucro.
Por lo tanto, en el cálculo de los costes de investigación también debería tenerse en cuenta la aportación del sector público (investigación básica realizada en universidades, fondos de investigación patrocinados por los Estados o por la Unión Europea) y sobretodo de la sanidad pública. ¿Cuántas ayudas públicas directas o indirectas ha concedido el sector público? ¿Quién paga los salarios de los profesionales que llevan a cabo proyectos de investigación y ensayos clínicos? El laboratorio da una cantidad por cada estudio, pero los costes fijos los paga la sanidad pública. Lo mismo que la analítica de control, o los cuidados de enfermería, etc. (Paul y Ankeny 2013). La cuestión es, entonces, cómo distribuir, cómo repartir los posibles beneficios de la I+D entre la empresa y el sector público (precios, beneficios, impuestos, participación en la propiedad, etc.).
A la hora de fijar el precio de un medicamento, se deberá descontar toda la inversión pública recibida específicamente para su investigación y desarrollo. Una fórmula alternativa sería incorporar a las entidades públicas en el accionariado de las empresas fabricantes en un nivel adecuado a la aportación en I + D realizada.
¿Se puede separar la I+D del precio? ¿Se puede financiar la investigación de otra manera? Indudablemente, se puede. La compensación del coste de la investigación incorporándola al precio, mediante la protección de la patente, no es el único mecanismo para estimular la innovación. De hecho, las patentes son un instrumento relativamente reciente, y la innovación se ha llevado a cabo desde el principio de la humanidad. La financiación privada de la investigación, a costa del propio investigador, de su familia, o de instituciones privadas, ha sido una fórmula bastante normal. Esa inversión se recuperaba, a veces, con la explotación del invento. También ha habido tradicionalmente financiación pública de la investigación. Este patrocinio ha tenido diferentes fórmulas: investigación intramural en centros de titularidad pública, becas o ayudas económicas, contratos públicos, o premios. Suzanne Scothchmer (2004) ha analizado con detalle las ventajas e inconvenientes de diferentes formas de financiación de la innovación.
En todo caso, la dificultad para imputar los gastos de investigación a los precios aumenta en una economía global, donde muchos países se benefician en diferente proporción. Por eso, una posible solución sería separar la financiación de la investigación y el desarrollo de la fijación de los precios. La Asamblea Mundial de la OMS discutió esta cuestión en 2008, lanzando una Estrategia Global y un Plan de Acción en relación con la Salud Pública, la Innovación y la Propiedad Intelectual. Se encargó a un Grupo de Expertos en Investigación y Desarrollo (CEWG) un Informe en el que se analizan diversas formas de financiar la I+D y se realizan propuestas interesantes, como innovación abierta, premios por pasos intermedios significativos, premios por resultado final, pool de patentes, etc. Los autores proponen el impulso de un Convenio internacional para la I+D de medicamentos, basado en el artículo 19 de la Constitución de la OMS, para identificar las prioridades de investigación, coordinar la investigación evitando duplicación de esfuerzos, y crear mecanismos para la financiación de la investigación y el desarrollo de medicamentos, que serían considerados bienes públicos y de dominio público (WHO 2012).
Las Conclusiones del Consejo de la Unión Europea sobre el rol de la UE en la Salud Global, de 10 de mayo de 2010 se refieren a esta materia en su punto 18. Se acuerda “(a) trabajar juntos para crear un marco global para la investigación y el desarrollo; (c) explorar modelos que separen el coste de la I+D de los precios de las medicinas”, etc. (Council of the European Union, 2010).
Si se financia la I+D por un mecanismo global y no se cargan esos costes en la industria, entonces la industria no tiene que financiar esos costes vía precios, y ya no tiene sentido la concesión de patentes para medicamentos. Aunque estas recomendaciones estaban pensadas para facilitar el acceso a medicamentos en países “en desarrollo”, la misma lógica se debe aplicar hoy a todos los países, ya que la sostenibilidad de los sistemas de salud y el acceso a los medicamentos está en juego también en los países llamados desarrollados con los precios de los “nuevos medicamentos”.
La propuesta de un Convenio Internacional y de la separación de la I+D del precio de los medicamentos es apoyada por otros expertos como Germán Velásquez (Velásquez G, 2013). También para Joseph Stiglitz la financiación de la innovación mediante “premios” sería más equitativa, aportando un fuerte impulso a la investigación, sin las ineficiencias asociadas con el monopolio (Stiglitz J, 2006).
Bloemen y Hammerstein (2012) insisten en la necesidad de separar los mecanismos de fijación de precios de la I+D y detallan acciones que debería abordar la Unión Europea para avanzar en esa dirección (Licencias Socialmente Responsables; Investigación de Fuentes Abiertas; Acceso Abierto; Cestas de Patentes; Parternariados en el desarrollo de patentes; Premios a la innovación; así como apoyar el desarrollo del Convenio Internacional).
Estos mecanismos requieren coordinación entre varios o muchos países, lo que a su vez genera costes. Pero en todo caso son estrategias que se deben explorar.
No es imposible. Conviene hacer notar aquí que, así como todavía no hay Acuerdos Internacionales (con sus sistemas de gestión correspondientes) para coordinar el gasto público en I + D, sí los hay para los Aspectos de los Derechos de la Propiedad Intelectual relacionados con el Comercio”, ADPIC o TRIPS (Scotchmer S 2006, pág 347). El problema para cambiar de modelo de financiación es que el sistema actual beneficia mucho a algunas industrias muy fuertes, con mucha capacidad de presión en los Gobiernos y Parlamentos nacionales y en la UE.
Otra situación que requiere atención es la financiación de los nuevos medicamentos para enfermedades de baja frecuencia. Si se carga en el precio toda la investigación de un nuevo producto (pongamos 100 millones de euros) y se va a aplicar solamente a 100 pacientes en el mundo, cada tratamiento costaría un millón de euros. Si la financiación de la investigación fuera por el sistema de premio (con un fondo global europeo o mundial), el medicamento solo tendría el precio del coste de fabricación. Si no se utiliza ese mecanismo, otra fórmula sería coordinar fondos nacionales o europeos para la financiación pública de estos medicamentos, con precios que incluyeran el coste de producción y el de I+D. La fuerza para cambiar de modelo tiene que venir de la convicción de mayorías importantes en todos los continentes, también en los países de ingresos altos, acerca de que la garantía del acceso a los medicamentos con el actual modelo no es sostenible, y no sólo para los más pobres.
La misma cuestión se plantea con la investigación en enfermedades de alta frecuencia pero en países de bajos ingresos, y también en medicamentos como los antibióticos, con poca expectativa de beneficio especulativo. El modelo de financiación de la I+D a través de precios especulativos bajo protección de patente no es eficaz para orientar la investigación hacia muchos problemas de salud pública de la humanidad.
En todo caso, se adopte uno u otro mecanismo para financiar la investigación, se debe asegurar una remuneración adecuada para los profesionales que realizan estas tareas, sea en la investigación básica o en la clínica. En el planteamiento que hacemos la financiación de la investigación queda garantizada, bien sea en el precio del medicamento innovador, al que se le incorpora el coste de la investigación, o bien sea en un fondo global (preferentemente internacional), si se separara este coste del precio de cada medicamento. El objetivo final que se pretende debe ser claro: reducir el precio injustificado de los medicamentos, el precio especulativo, que no guarda relación con los costes de la investigación ni de la fabricación.
Es importante hacer notar aquí que un sistema de patentes permite a las compañías farmacéuticas obtener la recompensa por la innovación mediante un mecanismo descentralizado; un aspecto que resulta particularmente relevante cuando las ventas se producen en muchos países distintos. Por lo tanto, cuando buscamos mecanismos alternativos debemos diferenciar entre mecanismos descentralizados y mecanismos centralizados que requieren la coordinación entre distintos países, lo que añade una complejidad notable. Soluciones descentralizadas pueden ser la reducción de la cobertura de la patente, permitiendo más competencia por otros productos, o la concesión de licencias obligatorias a nivel de país, que comentaremos después.
9.
La estrategia de algunas empresas en relación con las patentes y los precios.
Hay varias empresas farmacéuticas que han desarrollado o que están desarrollando medicamentos para la hepatitis C, y también están pidiendo precios muy elevados (más de 60.000€ por tratamiento como precio inicial). El método de cálculo del precio es el mismo, por el VALOR para la demanda, es decir, el máximo que el paciente, o el país, está dispuesto a pagar y puede pagar. Lo mismo ocurre con otros medicamentos de nueva generación para enfermedades neoplásicas, cardiovasculares, inflamatorias, neurológicas, etc. Como ya hemos señalado anteriormente los elevados precios fijados para los nuevos medicamentos limitan el acceso de los pacientes a los tratamientos, o ponen en riesgo la viabilidad de los sistemas de salud.
Algunas empresas llevan a cabo estrategias de discriminación de precios, fijando precios distintos para diferentes países, según su capacidad de pago, intentando captar máximo precio posible que ese país esté dispuesto y pueda pagar.
Este mecanismo no es necesariamente negativo, pero puede serlo. Si se quiere compartir el coste de la I+D entre los países que van a utilizar el producto, teniendo en cuenta que se deben pagar ciertos costes fijos, se puede buscar una forma de fijación de precios que conduzca al máximo valor social posible, a través de una discriminación positiva. El problema no es la existencia de discriminación de precios en sí. El problema es la discriminación de precios como expresión de “poder de mercado”.
En algunas ocasiones, en países que tienen cierta capacidad de pago y también capacidad de producir medicamentos genéricos, las empresas originarias conceden licencias voluntarias para la fabricación de genéricos. De esa manera limitan la presión para la concesión de licencias obligatorias o para la no concesión de patentes en ese país.
Estas políticas pueden limitar el acceso al medicamento a personas de países de rentas altas, pero también pueden ser ineficaces para aumentar el acceso en países de rentas medias o bajas, porque los precios sigan siendo demasiado altos para esas rentas.
En este sentido, Tracy Swan, Director del Proyecto Hepatitis/VIH del Grupo de Acción en Tratamientos de Nueva York, decía: “Es importante darse cuenta que las licencias voluntarias de Gilead son un lobo vestido de cordero. Van a limitar el acceso a millones de personas en situación de necesidad desesperada de tratamiento, y van a lesionar a toda la industria de genéricos” (Forette C, 2014). Hep Coalition y otras organizaciones plantean la necesidad de modificar estas políticas de licencias voluntarias para lograr la equidad real de acceso a los medicamentos contra la Hepatitis C (Forette C, 2015). Mediante esta estrategia de segmentación de mercado y licencias voluntarias se puede retrasar la competencia de genéricos sin licencia (en países donde no se haya concedido patente) o con licencia obligatoria.
En la Discusión sobre Competencia y Medicamentos Genéricos mantenida en el Comité de la Competencia de la OCDE (OECD 2014), se analizaron diversas formas en las que las empresas originarias intentan retrasar la entrada de genéricos: mejoras parciales del producto inicial para justificar nueva patente (“product hopping”), pago a empresas genéricas para no introducir el genérico (“pay for delay”), manipulación de las patentes, desinformación a los cuerpos reguladores y a los médicos, etc.
Algunas empresas intentan demorar la entrada de genéricos incluso cuando termina el tiempo de la patente inicial (“ever-greening”). La fórmula de los grupos de patentes, (“patent clustering”), promueve la solicitud patentes para diferentes elementos del producto o de su forma de administración. Se forman así clusters de varios cientos de patentes protegiendo un mismo producto.
También en la Unión Europea se ha propiciado la utilización de Certificados de Protección Suplementaria, que añaden 5 años de protección de la patente. Para ello se han utilizado argumentos contradictorios, como que servían para bajar los precios de los medicamentos y favorecían a la industria de genéricos, efectos que no se han observado en la práctica (De Boer 2015).
Otra estrategia empresarial denunciada por Médicos sin Fronteras, para controlar la utilización de genéricos, que podría vulnerar el derecho humano a la intimidad y la confidencialidad de la relación médico-paciente, es la exigencia de algunas empresas de conocer el nombre, la ciudadanía y el domicilio (con posible acceso a los datos clínicos) de los pacientes en tratamiento con alguna de las licencias voluntarias, arguyendo el objetivo de evitar el comercio paralelo (MSF 2015).
10.
Un mercado atractivo para los inversores.
En uno de los trabajos citados (Kantarjian 2014) se realiza una observación pertinente: en las declaraciones de Misión y de Visión de las empresas farmacéuticas suele definirse como objetivo principal la salud y el bienestar de los pacientes; este bienestar debe estar por encima de los criterios de los analistas financieros; este balance puede ser complicado.
Pero la cuestión se complica más cuando los propios dueños de los laboratorios farmacéuticos, sus principales accionistas, son las propias entidades financieras, los fondos de inversión. En este caso, la Misión y Visión de estas compañías es, lógicamente, la que prima, pasando a ser el medicamento otro producto financiero más, y teniendo como principal objetivo de la empresa la obtención de rentabilidad económica para los accionistas, con el consiguiente incentivo, fortísimo incentivo (decenas de millones de euros), en retribución y bonos para los altos ejecutivos.
Quizá aquí está parte de la causa de la escalada del precio de los medicamentos, que en 10 años se ha multiplicado por 10. En la fijación de precios de productos financieros influye la información que dichos precios dan a los mercados sobre expectativas de beneficio. El medicamento se transforma en un “generador de beneficios” para los accionistas.
El precio del producto farmacéutico es una “señal” para los mercados de valores. Si se baja el precio del medicamento y la expectativa de beneficio, baja el valor de las acciones y se debe desinvertir y cambiar de empresa o de sector. El inversor no tiene por qué tener un compromiso a largo plazo con el desarrollo de productos farmacéuticos o con los planes de salud de los países y sus necesidades. Evidentemente la situación es muy variada en diferentes empresas. Pero los bonos de los altos ejecutivos van ligados a la revalorización de las acciones y otras operaciones financieras, y los precios esperados son pieza clave en dichas operaciones.
Esta lógica de negocio colisiona, lógicamente, con la lógica de los sistemas de salud y los pacientes, que buscan obtener el acceso a los nuevos medicamentos, para atender a sus necesidades, al precio más bajo posible.
11.
¿Qué pueden (y deben) hacer los gobiernos, los Parlamentos y los demás agentes sociales? Los gobiernos deben abordar una serie de medidas complementarias. a) Negociación y fijación de precios más bajos.
En primer lugar, los gobiernos (en el caso de España y de los países miembros de la UE) deben fijar los precios de los medicamentos en función de los costes. Es la estrategia que puede dar resultados a corto plazo. Los gobiernos deben negociar con las empresas fabricantes el precio más favorable para el conjunto de la sociedad, de tal manera que se garantice a todos los pacientes el acceso a los medicamentos que necesiten.
- b) Reembolsar (financiar públicamente) los medicamentos que aporten valor y desinvertir (desfinanciar) los que no aporten va Los análisis de costo efectividad, costo beneficio, etc., deben utilizarse para decidir la inclusión o exclusión de un medicamento en la financiación pública.
- c) Concesión de licencias obligatoria
Si las empresas no aceptaran ajustar los precios a los costes, podría entenderse que hay un mal uso de la patente, ya que la finalidad de la patente no es el enriquecimiento de la empresa, sino la garantía de su estabilidad para mantener la investigación y desarrollo de nuevos medicamentos. En este caso, se debería conceder licencia obligatoria para que otras empresas pudieran fabricar de inmediato el medicamento. Esta estrategia puede dar frutos en un medio plazo, dependiendo de la tramitación de los decretos correspondientes y posible negociación con empresas. Ampliaremos el estudio de este mecanismo más abajo.
- d) Si no hubiera empresas privadas que quisieran fabricar el genérico a precio de coste, los gobiernos deberían organizar la producción a través de una empresa pública, al tratarse un riesgo para la salud pública. En este aspecto sería muy conveniente la coordinación entre países y financiadores de los sistemas de sa
- e) Las instituciones de la Unión Europea pueden jugar un papel más activo en este campo: -Se debería estudiar y, en su caso, desarrollar la utilización del mecanismo de compra conjunta de medicamentos por varios países de la Unión Europea para obtener mejores prec
-Las Agencias Nacionales y Europea de Medicamentos deberían desligar su financiación de la industria para ser más independiente en sus decisiones. El Grupo de Trabajo sobre Salud, Medicamentos e Innovación (2014) ha elaborado un decálogo de propuestas entre las que incluyen la necesidad de una evaluación de eficacia y seguridad independiente, transparente y participativa; la difusión de los datos de los ensayos clínicos; el acceso abierto a la literatura científica, etc.
-Si la UE legisla sobre patentes, como mecanismo de protección de la I+D, debería conocer los costes de producción de los medicamentos, y los precios, para poder valorar si hay o no un uso abusivo de las patentes. De ahí que sería conveniente un Comité Parlamentario encargado de esta cuestión.
-La UE debería ligar la financiación de proyectos de investigación a la concesión de Licencias Socialmente Responsables (Horizonte 2020) y debería impulsar el Convenio propuesto por la OMS para desarrollar mecanismos orientados a desligar la I+D de los precios.
-La Unión Europea debe explorar modelos para desligar el coste de la Investigación y el Desarrollo de los precios (Conclusiones del Consejo 10 mayo 2010). Esta estrategia puede rendir frutos en un medio-largo plazo, pero puede ser la solución más sólida, más eficiente y equitativa.
En este sentido la UE puede impulsar en la OMS la tramitación de un Convenio Internacional sobre investigación y desarrollo de medicamentos. Dicho Convenio tendría como objetivo el acceso a los medicamentos con unos precios razonables. Para ello la I+D se desligaría del precio (evitando la concesión de patentes) y se garantizaría mediante la fijación de prioridades de investigación (en función de las necesidades de salud), coordinación de la investigación, financiación mediante un fondo global.
- f) Además del papel decisivo de los Gobiernos y los Parlamentos, los diferentes agentes sociales deben promover (y deben participar en) la reforma de los sistemas de patentes relacionados con los medicamentos. Las organizaciones profesionales, las asociaciones de pacientes, los investigadores y las Universidades, los gestores sanitarios, los sindicatos, los partidos políticos, las Organizaciones no Gubernamentales y la industria farmacéutica originaria y de genéricos deben revisar la nueva situación y buscar las soluciones más justas y eficientes para la sociedad y para los pacien Es preciso recuperar un equilibrio justo.
Cabe citar aquí la reciente creación (27/1/2015) en el Parlamento Europeo de un Grupo de Interés sobre el Acceso de los pacientes a la Atención sanitaria con participación de Parlamentarios Europeos. En su primera reunión uno de los temas sobre los que se manifestó preocupación es la dificultad de acceso a los nuevos medicamentos en condiciones de igualdad para todos los ciudadanos europeos, sobretodo por el alto precio de los mismos.
La concesión de licencias obligatorias.
La cuestión se plantea con toda su crudeza cuando, como en el caso contemplado, es notorio y público que el precio del medicamento preciso para el logro o restauración de los pacientes, es claramente excesivo, por lo que no puede ser asumido por el Sistema Nacional de Salud Español, o, de otra manera, cuando el precio impide el normal funcionamiento del Servicio Público, sin que exista una verdadera justificación que derive de los costes del fármaco en cuestión.
Para evitar este tipo de situaciones los Estados acuden a diferentes remedios, entre los que sobresalen el relativo a las excepciones y limitaciones a los derechos conferidos por las patentes: licencias obligatorias y/o explotación por el Gobierno.
Sobre este particular es interesante la lectura del documento emitido por la Organización Mundial de la Propiedad Intelectual (OMPI), de 3 de noviembre de 20141. En dicho escrito se recoge la opinión de todos los países de la Organización Mundial de Comercio sobre el particular, incluida, naturalmente, España.
1 "Excepciones y limitaciones a los derechos conferidos por las patentes: licencias obligatorias y/o explotación por el Gobierno (Parte-1) documento preparado por la Secretaría. Comité permanente sobre el derecho de patentes, vigésima primera sesión. Ginebra, 3 a 7 de noviembre de 2014". Disponible en Internet SCP/21/4 REV.
Las causas por las que se pueden llevar a cabo dichas excepciones o limitaciones son las siguientes: 1) Impedir abusos de los derechos; 2) Establecer el equilibrio de intereses, 3) Promover el interés público en sentido amplío (España incluye la salud pública aunque no recoge específicamente lo que dispone la Ley india, esto es, que la invención patentada no esté disponible para la población a precios razonablemente asequibles o que los precios sean injustificadamente altos, ni tampoco lo que establece la Ley danesa, que es la imposibilidad de que la población acceda normalmente a los medicamentos), 4) Acabar con las prácticas anticompetitivas. Por estas prácticas entiende algún Estado que se refieren a la fijación de precios excesivos (Argentina) o a precios anormalmente altos de medicamentos (Francia). 5) El supuesto de emergencia nacional o circunstancias de extrema urgencia (salud pública, epidemias). 6) En fin, licencias obligatorias justificadas en caso de productos farmacéuticos (Austria, Nueva Zelanda, India, Brasil, Zambia y Zimbabwe).
Los acuerdos internacionales sobre esta cuestión avalan la capacidad de acción de los gobiernos. Así, quedó claro en la Conferencia de Doha con la Declaración sobre el Acuerdo sobre los Aspectos de los Derechos de la propiedad intelectual relacionados con el comercio, el “derecho de los miembros de la Organización Mundial de Comercio para usar, hasta el máximo, las previsiones del Tratado, que concede flexibilidad en su aplicación para proteger la salud” (WTO 2001). Se mencionan expresamente las situaciones de epidemia, pero no limita la concesión de licencias obligatorias a esta circunstancia ni a un tipo de país (de bajos ingresos). Se aplica a cualquier país, por lo tanto, también a España.
En resumen, se puede observar que los Estados, de una u otra manera, establecen ampliamente limitaciones o excepciones bajo diferentes causas, a los derechos conferidos por las patentes.
La Ley Española de patentes2 contempla la concesión de licencias obligatorias por motivos de interés público, incluyendo en estos la salud pública.
Sería conveniente, sin embargo, dado que en el momento actual se está produciendo la reforma de la Ley de Patentes, desglosar con toda claridad los supuestos de abusos de precio, tal y como lo han hecho otros Estados, no porque el sistema actual no sea suficientemente explícito, sino para que quede claro que dentro de la limitación actual, por razones de salud pública, se encuentra el mecanismo del abuso de precios, por posición dominante, derivada de la explotación de la patente.
Se trata, en estos casos, de hacer frente a las necesidades de un medicamento que añade de forma cuantitativa y cualitativa mayores esperanzas de vida y de curación, con lo que conecta con el derecho a la vida (Art. 15 de nuestra Constitución). El Tribunal Constitucional ha señalado que la garantía del derecho a la salud no sólo tiene una dimensión general asociada a la idea de salvaguarda de la salud pública, sino una dimensión particular conectada con la afectación del derecho a la salud individual de las personas receptoras. Este derecho subjetivo también se integra en el derecho a la vida.
2 Las referencias legales se han extraído del Texto consolidado publicado por el Boletín Oficial del Estado en Internet. (ley 11/1986, de 20 de marzo, con sucesivas modificaciones posteriores). Por otro lado, para lo que ahora interesa, no existe divergencia con el borrador del anteproyecto de Ley del Consejo de Ministros, también consultado en Internet.
La concesión de Licencias Obligatorias no se ha utilizado con mucha frecuencia, aunque sí en algunos casos.
Canadá la utilizó con relativa frecuencia. Según su legislación (Sección 41.3 de su ley de Patentes) el objetivo de la licencia obligatoria es “poner las medicinas a disposición del público al precio más bajo posible que sea congruente con remunerar adecuadamente al inventor por las investigaciones conducentes a la invención” (citada por Lobo F). Italia ha utilizado también esta posibilidad.
En los años 60 y 70 EEUU el ejército produjo tetraciclina y meprobamato sin autorización de los titulares de las patentes. En los 80 concedió licencia obligatoria para la fabricación de Insulina, y en los 90 para la fabricación de vacuna anti-rábica. En 2001 se consideró la posibilidad de conceder licencia obligatoria para la ciprofloxacina, pero Bayer, titular de la patente, decidió bajar el precio (Costa G 2006).
En Reino Unido se introdujo también el mecanismo de licencia obligatoria. Según el Departamento de Comercio “la mera presencia del artículo obraba “in terrorem” como medio para estimular la competencia vía precios y para evitar precios exorbitantes” (citado por Lobo F 1989).
La Fundación Salud Por Derecho también ha propuesto la utilización de licencia obligatoria para el caso de los nuevos medicamentos contra la Hepatitis C (Salud Por Derecho 2014).
- Conclusiones. a) Acceso El acceso a las medicinas que contribuyen a mantener y recuperar la salud y evitar la muerte prematura es un derecho humano fundamental.
- b) Precios Según sea el precio de los nuevos medicamentos, se puede acceder o no dichos medicamentos, y se puede poner en riesgo o no la viabilidad de los sistemas de salud.
El precio de los medicamentos en España lo fija el Ministerio de Sanidad, Servicios Sociales e Igualdad.
El precio fijado por las empresas para los nuevos medicamentos resulta injustificado y, con los datos conocidos hasta el momento, se pueden calificar de desorbitados.
La fijación de precio por “VALOR” (el precio más alto que alguien está dispuesto a pagar) y el establecimiento al mismo tiempo de la protección de la patente, que impide la competencia, lleva a los directivos de las empresas farmacéutica a forzar la negociación hasta obtener los precios más altos posibles que pueda pagar esa persona o esa economía nacional, incurriendo en abuso de posición dominante en el mercado.
Si una empresa quiere fijar los precios por VALOR (el máximo precio que alguien está dispuesto a pagar) el gobierno debe retirar de inmediato la protección de la patente, por abuso en la explotación de la misma, y debe estimular y garantizar la fabricación del medicamento a precio de COSTE (el precio más bajo al que se pueda producir, mediante genéricos con licencia obligatoria).
La fijación del precio de los medicamentos protegidos por patente en el Sistema Nacional de Salud debe hacerse siempre por el coste más bajo al que se pueda producir (por COSTE) y no al precio más alto que alguien esté dispuesto a pagar (por VALOR para la demanda).
- c) Patentes La patente es un instrumento social cuya finalidad es garantizar que la empresa innovadora recupere la inversión en investigación y desarroll No es un instrumento para generar el enriquecimiento mayor posible para la empresa.
La patente concedida se estaría utilizando de forma abusiva si una empresa aprovechara la posición dominante en el mercado para subir los precios hasta el límite máximo que el país pueda pagar.
- d) Legislación La legislación sobre patentes contiene elementos suficientes para hacer frente al problema planteado, mediante excepciones y limitaciones a los derechos conferidos por las patentes (licencias obligatorias y / o de explotación), de conformidad con los criterios establecidos por los diferentes países integrados en la Organización Mundial de la Propiedad Intelectual (OMPI).
Además de ser un problema de salud pública de primera magnitud, afecta a un derecho humano fundamental como es el derecho a la vida (Art. 15 de nuestra Constitución), entendido en un sentido amplio, tal y como lo ha recogido y repetido el Tribunal Constitucional, de manera que se pueda permitir a los pacientes acceder a aquellos medicamentos que permitan obtener el logro de su curación y garantizarles una calidad de vida asimilable a las personas sanas, utilizando al efecto la prestación farmacéutica a la que tienen derecho.
- e) Ámbito europe
La Unión Europea debe explorar modelos para desligar el coste de la Investigación y el Desarrollo de los precios (Conclusiones del Consejo 10 mayo 2010).
Se debe plantear la creación de un Comité Parlamentario para el análisis de los precios de los nuevos medicamentos Se debería ligar la financiación de proyectos de investigación a la concesión de Licencias Socialmente Responsables (Horizonte 2020).
- f) Ámbito mundia
La OMS debe agilizar la tramitación de un Convenio Internacional sobre investigación y desarrollo de medicamentos, en base al artículo 19 de su Constitución. Dicho Convenio tendría como objetivo el acceso a los medicamentos con unos precios razonables. Para ello la I+D se desligaría del precio (evitando la concesión de patentes) y se garantizaría mediante la fijación de prioridades de investigación (en función de las necesidades de salud), coordinación de la investigación, financiación mediante un fondo global.
- g) Consecuencias El gasto en exceso que se obliga a realizar al sistema de salud tiene como consecuencia el deterioro de otras funciones y, en caso de que este sistema de precios se consolidara para los nuevos medicamentos, pondría en riesgo la viabilidad de la sanidad pública a medio y largo p
- f) “No vale todo”.
En la fijación de precios de los nuevos medicamentos se han superado los límites de la prudencia. La conversión de los medicamentos en “productos financieros” y la fijación de los precios más altos que sea posible para obtener efectos en las cotizaciones y operaciones financieras derivadas, distorsiona la fijación de precios justos para un bien necesario para la salud de las personas. En el campo de la salud “no vale todo”.
No se debe, cuando está en juego la vida o la integridad de las personas, anteponer criterios económicos que hagan imposible o difícil el acceso a los medicamentos que impidan hacer frente, con garantías, a su enfermedad, de manera que se niegue directa o indirectamente las posibilidades de curación.
13.
Recomendaciones En el ámbito nacional.
A corto plazo.
1.Aprovechar la reforma de la ley de Patentes para especificar detenidamente los supuestos de excepción o limitación a los derechos derivados de la patente, incluyendo específicamente los supuestos de abuso de posición dominante, precios excesivos, etc. (El 16/6/2005 se publicó en el Boletín Oficial de las Cortes el texto aprobado en la Comisión de Industria del Congreso e inició su tramitación en el Senado).
2.Reducir drásticamente los precios de los nuevos medicamentos mediante la negociación con las empresas fabricantes, de manera que los precios se ajusten a los costes (incluyendo la investigación y el desarrollo) debidamente justificados y auditados, y garantizando un beneficio justo y prudente (10%). Condicionar el mantenimiento de las patentes a la fijación de dichos precios. Estas negociaciones no pueden eternizarse. Están en juego vidas humanas. Hay personas en España y en Europa que no pueden acceder a los medicamentos que necesitan porque ellos o sus sistemas sanitarios no pueden pagar el alto precio que exigen los fabricantes. Es llegado el tiempo de tomar decisiones sin más demora.
3.Establecer un control riguroso de la actuación de la Comisión de precios y del Comité Asesor, así como de los conflictos de intereses y régimen de incompatibilidades. Publicar las actas de dichos órganos colegiados con el fundamento de sus decisiones.
4.Exigir la total transparencia en el detalle de los costes de fabricación, así como de investigación y desarrollo (especificando posibles ayudas o participación pública en dicha investigación y desarrollo). Detallar qué beneficio esperado se incluye en el precio. Exigir la transparencia en los precios abonados por el sector público.
5.Descontar de los costes de producción de un medicamento, a la hora de fijar el precio, toda la inversión pública recibida específicamente para la investigación y desarrollo de dicho medicamento. Una alternativa a esta opción sería incorporar a las entidades públicas en el accionariado de las empresas fabricantes en un nivel adecuado a la aportación en I + D realizada.
6.Regular la publicación mensual del gasto farmacéutico hospitalario, de la misma manera que se conoce y publica el gasto mensual farmacéutico extra-hospitalario.
7.Promover un Comité Parlamentario, abierto a la opinión pública, para el análisis de los precios de los nuevos medicamentos.
8.Utilizar la evaluación costo-beneficio para rechazar la financiación pública de un medicamento que no aporte valor, pero no para fijar el precio (procedimientos de exclusión / inclusión).
A medio plazo.
9.En el caso de que no se logre un acuerdo inmediato para ajustar los precios a los costes, conceder licencias obligatorias y promover la fabricación de genéricos por otras empresas.
10.Si no hubiera empresas interesadas en la fabricación de genéricos, o se bloquearan estas iniciativas por las empresas originarias, organizar la producción de los genéricos en un laboratorio público.
11.Promover el análisis y, en su caso, la reforma de los sistemas de patentes relacionados con los medicamentos. Las organizaciones profesionales, las asociaciones de pacientes, los investigadores y las Universidades, los gestores sanitarios, los sindicatos, los partidos políticos, las Organizaciones no Gubernamentales y la industria farmacéutica originaria y de genéricos deben revisar la nueva situación y buscar las soluciones más justas y eficientes para la sociedad y para los pacientes.
Estimular en las Sociedades Científicas y los profesionales sanitarios la reflexión sobre su papel en la promoción de la utilización de nuevos medicamentos de altos precios, planteando el conflicto moral que supone la aceptación, sin discusión, de los altos precios exigidos por la industria, sabiendo que implican una reducción del acceso a estos medicamentos o a otros medicamentos y servicios necesarios, teniendo en cuenta que los recursos siempre son y serán limitados.
En el ámbito Europeo 12.Promover la actuación conjunta de los países miembros de la Unión Europea para diseñar una estrategia que garantice el acceso de la ciudadanía y de los pacientes, a los nuevos medicamentos y nuevos tratamientos innovadores, acordando una reducción drástica de los precios de los medicamentos innovadores.
13.Valorar e impulsar la utilización los mecanismos coordinados de compra.
14.Valorar la posibilidad de reducir el tiempo de protección de la patente y la posibilidad de retirar la patente en el caso de uso abusivo.
Para garantizar que la patente sirve a la finalidad social para la que se creó (financiar los costes de la I+D de la empresa innovadora) es indispensable conocer los Costes, los Precios (que deben cubrir los costes) y un beneficio prudente. Si no se tiene esta información se cae en el riesgo de un uso abusivo de patente porque la autoridad que la concede no puede controlar su uso.
Se debe plantear la creación de un Comité Parlamentario para el análisis de los precios de los nuevos medicamentos. Exigencia de transparencia.
15.Vincular la financiación de I+D (Horizon 2020, etc.) al establecimiento de Licencias socialmente responsables. Promover una estrategia mundial en esta materia.
La Unión Europea debe explorar modelos para desligar el coste de la Investigación y el Desarrollo de los precios (Conclusiones del Consejo 10 mayo 2010).
Desligar la financiación de las Agencias reguladoras (Agencia Europea del Medicamento) de la industria farmacéutica (actualmente el 83% de su presupuesto lo paga la industria con las tasas de tramitación de las autorizaciones). Control estricto de conflicto de intereses.
En el ámbito Mundial 16.Promover un Convenio de la OMS para la I+D de medicamentos, estableciendo mecanismos para la fijación de prioridades, la coordinación de los esfuerzos de I+D y la creación de un fondo global público (ámbito Europeo o Mundial) para la financiación de la investigación de nuevos medicamentos, desligando este factor de los sistemas de fijación de precios. Este fondo financiaría directamente investigación o bien compraría patentes de medicamentos desarrollados por una industria. De esta forma se autorizaría de forma inmediata la fabricación de genéricos y se podrían incorporar los nuevos medicamentos que fueran efectivos, separando el coste de la investigación del precio del producto.
Otras alternativas.
Este tema tan complejo y que afecta a un tema tan importante como la salud puede beneficiarse de otras aportaciones que personas afectadas, agentes sociales, universidades y profesionales puedan realizar. Las aportaciones a este documento serán bienvenidas.
Los Estados Miembros deberfan explorar modelos que disocien el Coste de Ia 1+0, de los precios de los medicamentos...
... y asegurar que las inversiones de Ia UE en investigaci6n sanitaria garantizan el acceso al conocimiento y a las herramientas generadas como bien publico global, ayudando a generar medicamentos esenciales a precios asequibles, para ser usados de forma racional [Conclusiones del Consejo de Ia Union Europea sobre el rol de Ia Union Europea en Ia Salud Global, 10 mayo 2010]
- REFERENCIAS Bañuelos J (2015) Gilead admite que ha cuadruplicado sus beneficios gracias a Sovaldi. Cadena Ser 4/2/2015 http://cadenaser.com/ser/2015/02/04/sociedad/1423064456_083177.html Bañuelos J (2015-2) El creador de Sovaldi: “España no puede dejar morir a sus pacientes”. Cadena Ser 30/1/2015 http://cadenaser.com/ser/2015/01/30/sociedad/1422623805_535040.html Bennett J D (2014). Affording specialty medicines. Timesunion.com 19 Nov 2014. http://www.timesunion.com/opinion/article/Affording-specialty-medicines- 5901631.php Bloemen S, Hammerstein D (2012). Time for the EU to lead on innovation. EU policy opportunities in biomedical innovation and the promotion of public knowledge goods. Health Action International, Trans Atlantic Consumer Dialogue. Netherlands, April 2012.
http://tacd-ip.org/wp-content/uploads/2012/04/Final-Paper-Time-for-the-EU-to-lead-on- new-innovation-models_April-16-TIMES-NEW-ROMAN.pdf BOC (2015) Proyecto de Ley de Patentes 121/000122. Boletín Oficial de las Cortes Generales. Congreso de los Diputados. Serie A: Proyectos de Ley. 28 de noviembre 2014. Núm. 122-1.
CESCR (2001) Human Rights and intellectual property. E/C 12/2001/15 CESCR (2005) Committee on Economic, Social and Cultural Rights. General Comment Nº17. The right of everyone to benefit from the protection of the moral and material interests resulting from any scientific, literary or artistic products of which he or she is the author (article 15, paragraph 1(c), of the Covenant) Chimicles N E et al (2014) Southeastern Pennsylvania Transportation Authority (plaintiff) v. Gilead Sciences, Inc (defendant); United States District Court for the Eastern District of Pennsylvania. December 9 2014.
CNMC (2015) Informe sobre el Proyecto de Real Decreto Legislativo por el que se aprueba el Texto Refundido de la Ley de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios. IPN/CNMC/005/15. Comisión Nacional de los Mercados y la Competencia. 12 marzo 2015.
Costa G (2006). Patentes Farmacéuticas: ¿Por qué dificultan el acceso a los medicamentos? Asociación Brasileña Interdisciplinaria de SIDA, Río de Janeiro, 2006.
Council of the European Union (2010). Council conclusions on the EU role in Global Health, 10 may 2010.
http://ec.europa.eu/health/eu_world/docs/ev_20100610_rd04_en.pdf Danzon P and Pauly M (2002). Health Insurance and the growth in pharmaceutical expenditures. Journal of Law and Economics, vol XLV (October 2002): 587-613.
De Boer (2015). Supplementary Protection Certificate for medicinal products. An assessment of European Regulation. Vrije Universiteit. Amsterdam.
Di Masi JA, Hassen RW, Grabowski HG (2003). The price of innovation: new estimates of drug development costs. J Health Econ 2003; 22: 151-185 DiMasi JA et al (2014). Innovation in the pharmaceutical industry: new estimates of R&D costs. Tufts Center for the Study of Drug Development, Boston.
Dna (2015) Natco wins India regulator nod for Sovaldi generic, Mumbai 13/3/2015 http://www.dnaindia.com/money/report-natco-wins-india-regulator-nod-for-sovaldi- generic-2068384 DNDi (2014). An innovative approach to R&D for neglected patients. Ten years of experience & lessons learned by DNDi. Drugs for Neglected Diseases initiative, January 2014.
EASL (2014) European Association for the Study of the Liver. Clinical Practice Guidelines: Management of hepatitis C virus infection. Journal of Hepatology 2014; 60: 392-420 http://www.easl.eu/assets/application/files/bdb06ff135c7ccb_file.pdf European Commission (2009) European Competition Pharmaceutical Sector Inquiry Ferreira A (2014) Hepatite C e o meganegócio farmacêutico. Journal de Noticias 10.12.2014.
Forette C (2014) Gilead’s license on Hepatitis C drugs, Sofosbuvir and Ledipasvir: a Fool’s Bargain. Hep Coalition, 10 october 2014 http://www.hepcoalition.org/advocate/advocacy-tools/article/gilead-s-license-on- hepatitis-c?lang=en Forette C (2015) Equitable access to HCV drugs. Hep Coalition, 22 April 2015 http://hepcoalition.org/advocate/campaigns/article/equitable-access-to-hcv-drugs- 183?lang=en Gotzsche P (2014) Medicamentos que matan y crimen organizado: cómo las grandes farmacúticas han corrompido el sistema de salud. Los libros del lince, Barcelona 2014 Grupo de Trabajo sobre Salud, Medicamentos e Innovación (2014). Compromiso europeo por el desarrollo de la salud y el acceso a los medicamentos. Decálogo para las diputadas y diputados del Parlamento Europeo. Noviembre 2014. http://saludporderecho.org/wp-content/uploads/2014/11/DECALOGOGTSMI-esp.pdf
Hecketsweiter Ch, Benkimoun P (2015). Hépatite C: bataille pour l’accès à un traitment révolutonnaire. Le Monde édition globale 22.1.2015 HepCoalition (2015) http://www.hepcoalition.org/news/article/gilead-s-license-on-hepatitis-c?lang=en Hill A et al (2014). Minimum costs for providing Hepatitis C Direct Acting Antivirus for use in large-scale treatment access programs in developing countries. Clinical Infectious Diseases Advance Access publication February 13, 2014.
I-MAK (2015). Gilead denied patent for Hepatitis C drug Sofosbuvir in India. Initiative for Medicines, Access and Knowledge. 14 Jun 2015.
http://www.i-mak.org/news-releases/ IMS Institute for Healthcare Informatics (2014). Global Outlook for Medicines Through 2018. November 2014.
Kanavos P. Short –and Long- Term Effects of Value-Based Pricing vs External Price Referencing. Eminet. LSE, 2010 http://ec.europa.eu/enterprise/sectors/healthcare/files/docs/valuebased_pharmapricing_0 12010_en.pdf Kantarjian H et al (2013-1). The Price of Drugs for Chronic Myeloid Leukemia (CML); A Reflection of the Unsustainable Prices of Cancer Drugs: From the Perspective of a Large Group of CML Experts. Blood first edition paper, prepublished online April 25, 2013; doi 10.1182/bood-2013-03-490003 Kantarjian H e al (2013-2). Cancer Drugs in the United States: Justium Pretium – The Just Price. Journal of Clinical Oncology. Published online ahead of print on May 6, 2013 as DOI: 10.1200/JCO.2013.49.1845 Kantarjian H et al (2014). High Cancer Drug Prices in the United States: Reasons and Proposed Solutions. Journal of Oncology Practice. July 2014, Vol 10 (4): e208-e211 Kotler P (1991). Marketing Management. Prentice-Hall, New Jersey.
Lago C (2015). Osakidezta tratará a todos los pacientes de hepatitis C pero de forma escalonada. Noticias de Gipuzkoa. 15 mayo 2015. http://www.noticiasdegipuzkoa.com/2015/05/15/sociedad/osakidetza-tratara-a-todos- los-pacientes-de-hepatitis-c-pero-de-forma-escalonada Lamata F et al (1994) Marketing Sanitario. Díaz de Santos. Madrid, 1994.
Lamata F y Galvez R (2015). Hepatitis C: presupuestos suficientes y precios razonables. Público, 5.1.2015.
Ley 11/1986, de 20 de marzo, de Patentes. BOE núm 73, de 26 de marzo de 1986. BOE-A 1986-7.900, modificada por Ley 10/2002 de 29 abril.
Light DW, Warburton RN (2011). Demythologizing the high cost of pharmaceutical research. Biosocieties, 2011; 6: 34-50, doi: 10.1057 / biosoc. 2010.40. published online 7 Feb 2011.
Light DW, Kantarjian H. Market spiral pricing of cancer drugs. Cancer 2013 Nov; 119 (22): 3900-3902. doi: 10.1002/cncr.28321 http://onlinelibrary.wiley.com/doi/10.1002/cncr.28321/abstract;jsessionid=C56893E6A 8DE26DC7C1A17D7CCF89000.f04t01 Lobo F (1989) La evolución de las patentes sobre medicamentos en los países desarrollados. Doc. nº 009/1989 (Ponencia presentadas en la “Reunión de consulta sobre la industria farmacéutica Latinoamericana” organizada por el Sistema Económico Latinoamericano –SELA- Caracas 11 al 13 de Mayo de 1988).
Martínez Olmos J (2015). La sanidad del futuro a propósito de la Hepatitis C. Amarppe, 2015.
MdM (2015) Doctors of the World opposes the patent on sofosbuvir. “Hepatitis C: scourge, remedy and scandal”. February 2015.
Mestre-Ferrandiz J, Sussex J and Towse A (2012) The R & D Cost of a new medicine. Office of Health Economics. London, 2012.
Moital I et al (2014) El caso Glivec: primer ejemplo de debate global en torno al sistema de patentes de medicamentos. Gaceta Sanitaria 2014; 28(6): 470-474 MSF (2015). Barriers to access and scale up of hepatitis C (HCV) Treatment: Gilead’s anti-diversion programme. Médecin Sans Frontières briefing document, January 2015.
MSSSI (2015). Plan estratégico del abordaje de la Hepatitis C. Ministerio de Sanidad, Servicios Sociales e Igualdad. 2015. http://www.msssi.gob.es/gabinete/notasPrensa.do?id=3576 Novoa A (2014). Las patentes de los medicamentos. Relato de un gran fracaso político. Rebelión, 22.11.2014 NYT (2013). The cost of living. New York Times, 2013. http://nymag.com/news/features/cancer-drugs-2013-10/index1.html OECD (2014). Summary Record of the Discussion on Competition and Generic Pharmaceuticals. Annex to the Summary Record of the 121st Meeting of the Competition Committee held on 18-19 June 2014. http://www.oecd.org/officialdocuments/publicdisplaydocumentpdf/?cote=DAF/COMP/ M(2014)2/ANN3/FINAL&doclanguage=en OECD (2014-2). Health at a Glance: Europe 2014. OECD 3 Dec 2014 http://www.oecd-ilibrary.org/social-issues-migration-health/health-at-a-glance- europe_23056088
OMC (2015-1). La financiación de medicamentos innovadores para la Hepatitis C. Comunicado de la Organización Médica Colegial. 19.1.2015.
OMC (2015-2). Medicamentos: visión social y clínica. Documento aprobado por unanimidad por la Asamblea General de la Organización Medica Colegial el 28.3.2015.
Paul DB, Ankeny RA. Patenting the PKU Test – Federally funded research and intellectual property. N Engl J Med 2013; 369: 792-794 http://www.nejm.org/doi/full/10.1056/NEJMp1306755 Pear R (2015). Obama Proposes That Medicare Be Given the Right to Negotiate the Cost of Drugs. The New York Times, April 28, 2015. New York edition, page A16.
Pita Barros P (2014) “Hepatite C e o meganegócio farmacêutico”, por Antonio Ferreira.
Blog de Pedro Pita Barros 11.12.2014 Pita Barros P (2015) Hepatite C, novamente. Blog de Pedro Pita Barros 7.1.2015 PlafHc (2015) Plataforma de personas afectadas por Hepatitis C. Spanish Hepatitis C Patients Petition European Parliament. IP Policy Committee blog. 25 Jan 2015. http://tacd-ip.org/archives/1282 PlafHc (2015-2) La Plataforma de enfermos de hepatitis C traslada su denuncia a la Eurocámara. Agencia EFE, Bruselas, 22 enero 2015. http://www.euroefe.com/3790_economia-y-empleo/2892408_la-plataforma-de- enfermos-de-hepatitis-c-traslada-su-denuncia-a-la-eurocamara.html PlafHc (2015-3) Afectados por Hepatitis C denuncian en el Tribunal Supremo 2 homicidios y 37 lesiones por no recibir medicamentos. Agencia Europa Press, Madrid, 13 Febrero 2015.
http://www.europapress.es/madrid/noticia-afectados-hepatitis-denuncian-tribunal- supremo-homicidios-37-lesiones-no-recibir-medicacion-20150213144530.html Prescrire Int (2011) New drugs and indications 2010: indadequate assessment; patients at risk. Prescrire Int 2011: 20(115): 105-110 http://english.prescrire.org/en/115/446/48385/2403/2399/SubReportDetails.aspx Real Decreto-ley 16/2012, de 20 de abril, de medidas urgentes para garantizar la sostenibilidad del Sistema Nacional de Salud y mejorar la calidad y seguridad de sus prestaciones. BOE núm 98, de 24 de abril de 2012, páginas 31278 a 31312.
Rovira J, Gómez P, del Llano J (2012). La regulación del precio de los medicamentos en base al valor. Fundación Gaspar Casal; Laboratorios Lilly.
Sachs J (2015) The drug that is bankrupting America. The Blog. Huff Post Business.
16/2/2015.
Salud Por Derecho (2014) Sin acceso a una cura para la hepatitis C. El problema no es el presupuesto, es el precio.
http://saludporderecho.org/wp-content/uploads/2015/02/HepC-Briefing-Esp.pdf
Sánchez Caro J, Abellán F (2014). Bioética de las patentes relacionadas con la salud. Fundación Salud 2000. Madrid, 2014.
Santoro A, Mazza R, Carlo-Stella C.Early response or clinically meaningful results to drive chronic myeloid leukemia therapy? Re: “Early response with dasatinib or imatinib in chronic myeloid leukemia: 3-year follow-up from a randomized phase 3 trial (DASISION)” Jabbour, et al., 123:494-500 doi:10.1182/blood-2013-06-511592 Scotchmer S (2006). Innovation and Incentives. MIT Press, 2006 Silverman E (2015). “We need a petititon” to lower cancer drug prices: Kantarjian explains. Pharmalot. The Wall Street Journal, 23 Feb 2015.
Stiglitz J (2006) Give prizes not patents. New Scientist 16 Sept 2006: 21 The Economist (2015). An introduction to value-based healthcare in Europe. The Economist Intelligence Unit 2015. http://www.economistinsights.com/sites/default/files/An%20introduction%20to%20val ue-based%20healthcare%20in%20Europe.pdf The Lancet (2015). Editorial. “Hepatitis C: only a step away from elimination? www.thelancet.com Vol 385 March 21, 2015.
Van de Vooren K, Curto A, Garattini L (2015). Pricing of forthcoming therapies for hepatitis C in Europe: beyound cost-effectivenes? Eur J Health Econ (2015) 16: 341- 345.
Velasquez G (2013). ¿Hacia un tratado internacional para la investigación farmacéutica? Una reforma necesaria. Le Monde Diplomatique, abril 2013 Ventayol P (2015). Opinión en “Algunas formas de analizar los nuevos tratamientos de la Hepatitis C. Economía y Salud. Boletín Informativo, 2015. Abril, nº 82. http://www.aes.es/boletines/news.php?idB=23&idN=1337 WHA (2015) World Health Assembly addresses antimicrobial resistance, immunization gaps and malnutrition. News releases, 25 May 2015. http://www.who.int/mediacentre/news/releases/2015/wha-25-may-2015/en/ WHO (2012) Research and Development to Meet Health Needs in Developing Countries: Strengthening Global Financing and Coordination. Report of the Consultative Expert Working Group on Research and Development: Financing and Coordination. World Health Organization, 2012.
WHO (2012-2) Sixty-Fifth World Assembly, Geneva 21-26 May 2012. Resolutions and Decisions. WHA 65 22 Resolution: Follow-up of the report of the Consultative Expert Working Group on Research and Development: financing and coordination. Pag 37-38.
WHO (2015). New Model essential medicines list published today. http://www.who.int/medicines/news/eml_2015/en/ WHO (2015-2) Access to new medicines in Europe: technical review of policy initiatives and opportunities for collaboration and research. WHO, Regional Office for Europe, March 2015.
WHO, WTO, WIPO (2013) World Health Organization, World Trade Organization, World Intellectual Property Organization. Technologies and Innovation. Intersetions between health, intellectual property and trade.
WIPO (2004). Handbook on intellectual property. World Intellectual Property Organization 2004, reprinted 2008.
WTO (1994) Agreement on Trade-Related Aspects of Intellectual Property Rights, 15 April 1994.
WTO (2001) Declaration on the TRIPS agreement and Public Health, Doha 14 Nov 2001.





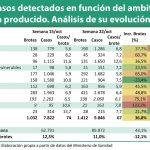















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: