
Los conjuntos de Precios de Referencia pueden estar formados por medicamentos constituidos por sales o ésteres diferentes de las del medicamento original, así como por productos que tengan como vía de administración cualquiera de las consideradas como parenterales, es decir, intramuscular, la subcutánea, intravenosa, entre otras. Así lo ha establecido el Tribunal Supremo en una sentencia en la que rechaza un recurso contencioso-administrativo presentado por Farmaindustria en el que cuestionaba la formación de conjuntos afectados por estas dos situaciones.
El Supremo rechaza ambas motivaciones de plano y desestima el recurso que la patronal presentó contra la Orden SSI/1225/2014, de 10 de julio, por la que se procede a la actualización del sistema de precios de referencia de medicamentos en el Sistema Nacional de Salud, y la declara conforme a Derecho, confirmándola. Farmaindustria había señalado que en la orden impugnada se habían “formado conjuntos con presentaciones de medicamentos que no tienen el mismo principio activo por cuanto difieren en las sales unidas al mismo principio activo, por lo que difieren en cuando a su eficacia farmacológica”. Algunos de los conjuntos impugnados eran el C74 referido al ibuprofeno respecto del ibuprofeno-arginina; C164 referido al ácido micofenólico respecto de micofelonato de mofetilo; C270 referido al ciclopirox respecto del ciclopirox olamina; H75 referido a la toxina botulínica tipo A y la de tipo B.
Por otro, la patronal señaló que en los conjuntos se han incluido presentaciones en los que figura como vía de administración la ‘vía parenteral’ que no constituye una única vía de administración pues puede tratarse de inyecciones intramusculares, subcutáneas, endovenosas, etc. En este sentido, los conjuntos impugnados eran C304 (epinefrina), C422 (triptorelina) y C342 (Insulina soluble neutra humana).
El TS rechaza todas las alegaciones de la patronal, tanto en lo que respecta a la denominación y clasificación de medicamentos. El Tribunal considera que hay que distinguir el régimen de autorización, el de formación de conjuntos y el de dispensación y, en su caso sustitución. Aspecto este último “al que hay que referir el régimen de agrupación de medicamentos, no es ahora relevante”, explica.
A los efectos de la formación de conjuntos y que éstos deban hacerse con medicamentos que cuenten con el mismo principio activo, es relevante según el Supremo “que respecto de los genéricos el artículo 8.g) de la Ley del Medicamento prevea que “las diferentes sales, ésteres, éteres, isómeros, mezclas de isómeros, complejos o derivados de un principio activo se considerarán un mismo principio activo”. Además, el Alto Tribunal avala la utilización de la clasificación ATC y en concreto el nivel ATC 5 para la configuración de conjuntos a pesar de que, como explica Farmaindustria, “diversas entidades farmacológicas que se encuadran en el mismo nivel 5 no responden al mimo principio activo”.
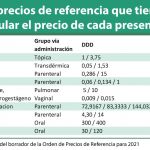
Con respecto a la vía de administración el Supremo considera que “en la Directiva 2001/83/CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se establece un código comunitario sobre medicamentos para uso humano, la "vía parenteral" se identifica en el artículo 71.1 , último guión, como vía de administración”. Además, explica que la Agencia Española de Medicamentos (Aemps) en sus directrices para la “elección del nombre de los medicamentos de uso humano, las vías de administración se designarán utilizando los términos estándar en español publicados por la Dirección Europea para la Calidad de los Medicamentos (EDQM) del Consejo de Europa. Según tal instrumento el método de administración o AME-0011 Injection se refiere a la administración de un fármaco en el cuerpo, usualmente tras hacer una punción y se remite como vías más comunes a la intravenosa, intramuscular y subcutánea”. En este aspecto, la sentencia señala que el perito manifestó en el acto de ratificación que "vía parenteral" equivalía a inyección.
Por último, el tribunal señala que en otros casos sí que se ha rectificado la orden, diferenciado vías de administración oral como bucal, sublingual u oral.





















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: