El Boletín Oficial de la Comunidad Foral de Navarra recoge hoy, 16 de noviembre, la Orden Foral 622E/2017, de 9 de octubre, por la que la Consejería de Salud establece los requisitos técnico-sanitarios aplicables a la preparación y entrega de los sistemas personalizados de dosificación (SPD) de medicamentos en las oficinas de farmacia, en línea con lo dispuesto en el artículo 86 del Real Decreto Legislativo 1/2015 que aprueba el texto refundido de la Ley de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios. Básicamente, lo que hace esta orden es fijar los criterios relativos a locales, equipamiento y utillaje, documentación y personal, para "garantizar", dicen, "que la actividad de reacondicionamiento de medicamentos se lleva a cabo bajo condiciones adecuadas de calidad".
Primeramente, se establece la necesidad de informar al paciente sobre la actividad y su objetivo, y recabar su consentimiento informado, o, en caso de dependencia, del del familiar, cuidador o representante legal. También se detallan las intervenciones a realizar, incluyendo la recogida de información clínica y farmacológica; la revisión del tratamiento para detectar posibles problemas relacionados con los medicamentos, la elaboración de la documentación necesaria; la preparación; el control de calidad; la entrega de los dispositivos y la información correspondiente y el seguimiento farmacoterapéutico, atendiendo a los posibles cambios de medicación.
Seguidamente, se detallan los criterios de inclusión. Básicamente, aquellos medicamentos que por sus características pueden permanecer estables en el dispositivo durante el tiempo previsto para su utilización, entre los que no están los higroscópicos, fotosensibles, comprimidos dispersables, efervescentes o sublinguales, ni ningún otro cuya ficha técnica especifique que se debe conservar en el envase original. Además, se establece un periodo máximo de dos semanas de tratamiento (salvo excepciones), con el fin de garantizar la estabilidad de los medicamentos y la revisión de la medicación, teniendo en cuenta los posibles cambios. Preferentemente, dice la Orden, se utilizará el SPD con "pacientes con problemas de incumplimiento de la terapia o de utilización incorrecta de los medicamentos: polimedicados, mayores con problemas de organización de los medicamentos, personas que viven solas, las incluidas en programas de mejora en el cumplimiento y también a las que el médico vea como susceptibles de recibir este dispositivo de ayuda".
En cuanto al acondicionamiento de los locales, se exige a las farmacias que quieran hacer SPD contar con un laboratorio o zona de preparación diferenciada, libre de obstáculos y con control de temperatura y humedad (15-20º/40-60%), con una superficie de trabajo lisa, lavable y desinfectable y con un tamaño suficiente, con un área de almacenamiento para el material, la medicación y la documentación, y un área de atención farmacéutica individualizada que garantice la confidencialidad.
Equipamiento y personal
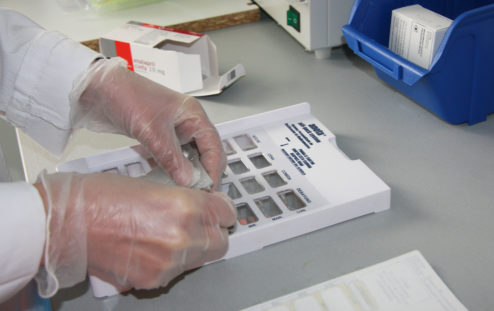
Como equipamiento necesario, la Orden obliga a tener dispositivos homologados y certificados por el fabricante, además de un sistema adecuado para el sellado y cierre de los dispositivos, utillaje para fraccionar las unidades, pinzas para manipularlas, recipientes cerrados para almacenar la medicación restante identificados con el nombre del paciente, un sistema de archivo para la documentación. También se establece que el personal deberá llevar bata, gorro, mascarilla y guantes desechables.
Además de esto, se pide a las farmacias que dispongan de un Procedimiento Normalizado de Trabajo (PNT), en el que queden contempladas la asignación de funciones y responsabilidades, la higiene necesarias, la formación del personal (todos los participantes en la preparación deberán contar con formación específica y se nombrará a un responsable), la limpieza y el control de las condiciones ambientales del local, el mantenimiento del equipamiento, la recepción y almacenamiento de los dispositivos, y una descripción detallada del proceso, desde la información hasta la entrega al paciente, incluyendo un registro de actuaciones, entre otros aspectos.
En cuanto al seguimiento farmacoterapéutico, se establece como documento base la hoja de prescripciones del sistema de receta electrónica. Además, se registrarán en la ficha datos del paciente, el médico prescriptor, los medicamentos prescritos, posibles alergias, contraindicaciones o reacciones adversas, y posibles problemas relacionados con la medicación, incidencias e intervenciones del farmacéutico.
Garantizar la trazabilidad
De cara a garantizar la trazabilidad, se registrará también un número de registro interno del SPD, nombre del paciente, fecha de preparación, datos de los medicamentos acondicionados, del material, duración del tratamiento, así como la identificación del responsable de la elaboración, la fecha de entrega y las posibles incidencias. Los dispositivos deberán llevar un etiquetado legible en el que se identifique el establecimiento farmacéutico y sus datos de contacto, así como el nombre del paciente, el número de registro interno, y la fecha de inicio y de final del blíster, en la cara anterior; y el nombre de el medicamento, posología, momento de la administración, aspectos físicos de identificación de los medicamentos y lotes en la posterior. También se podrá entregar una ficha adjunta con los datos básicos para identificar a los agentes implicados, datos de contacto e instrucciones para la conservación y manipulación del SPD.
La Orden establece que la actividad podrá iniciarse desde el día de la presentación de la declaración responsable (de renovación obligatoria cada cinco años), en la que el titular certifica el cumplimiento de los requisitos de su establecimiento. Las farmacias que ya estuvieran acreditadas para la preparación de SPD podrán continuar con la actividad, debiendo adecuarse a la normativa y presentar una declaración responsable. También se prevé la imposición de sanciones administrativas para quienes realicen la actividad sin disponer de ella, o falsee u omita datos en la misma.






 Lilisbeth Perestelo:
Lilisbeth Perestelo:  César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):