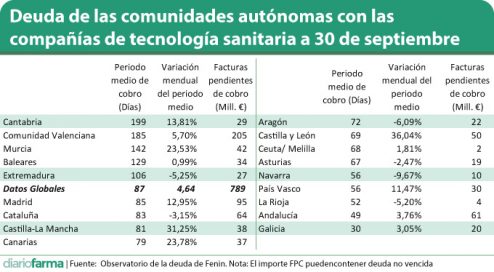
La Federación Española de Empresas de Tecnología Sanitaria (Fenin), ha hecho pública la cifra global de facturas pendientes de cobro (FPC) de las comunidades autónomas por parte de las compañías de este sector, recogidos en el 'Observatorio de la deuda de Fenin', que se habría situado en los 789 millones de euros en los primeros nueves meses de este año, lo que, indica, dicen, un aumento del 3,5% (27 millones) con respecto al primer semestre de 2018.
Asimismo, señalan que el periodo medio de pago ha subido en 13 días en relación con el primer semestre, al pasar de los 74 a los 87 días. Según reflejan los datos del Observatorio, el 79,1% de las facturas pendientes de cobro corresponden al ejercicio 2018 y el 20,9% restante al de 2017 y anteriores.
No obstante, como viene siendo habitual en las comunicaciones que realiza la patronal en relación con la deuda, ésta señala a las comunidades autónomas con menos de 60 días de pago, es decir, con plazos ajustados a la ley, y destaca, en este apartado, a Galicia, con 30 días; Andalucía, con 49; La Rioja, con 52, y País Vasco y Navarra, ambas con 56. Asturias, Ceuta y Melilla, Castilla y León, Aragón, Canarias, Castilla-La Mancha, Cataluña, Madrid y Extremadura se sitúan entre los 60 y los 120 días, mientras que Cantabria (199), Comunidad Valenciana (185), Murcia (142) y Baleares (129) siguen superando, con distinta amplitud, esas cifras.
Nueva normativa europea
De la actualidad que afecta al sector de las tecnologías sanitarias está, más allá de la deuda, la aplicación a nivel nacional de lo dispuesto por los reglamentos europeos 2017/745 sobre productos sanitarios y 2017/746 sobre productos sanitarios para el diagnóstico in vitro, que entrarán en vigor el próximo 20 de mayo de 2020 y 26 de mayo de 2022, respectivamente, y obligarán a un desarrollo normativo en España.
Así, la secretaria general de Fenin, Margarita Alfonsel, señalaba recientemente que "los fabricantes de tecnología sanitaria están llevando a cabo grandes inversiones para actualizar toda la documentación técnica que les permita cumplir con los nuevos reglamentos". No obstante, el sector aguarda a que la Comisión Europea y los Estados miembros pongan en marcha toda la infraestructura necesaria para el funcionamiento del nuevo sistema normativo. Y, en este sentido, se refirió a "la redesignación de los organismos notificados responsables de la evaluación y (re)certificación de la mayoría de los productos sanitarios y de los productos sanitarios para diagnóstico in vitro para que puedan ser comercializados en la Unión Europea”.
A este respecto, la directora técnica, María Aláez, aseguró que "los nuevos reglamentos incluyen requisitos aún mayores para los organismos notificados y aplican a un mayor número de productos". De ahí que sea necesario, apuntó, "que se establezca con suficiente antelación un sistema de organismos notificados plenamente funcional, con la capacidad y la experiencia necesarias para cumplir con los nuevos requisitos y poder gestionar la carga de trabajo de acuerdo con el marco normativo actual y futuro". Sobre esto, cabe destacar que Mª Carmen Abad, jefa del departamento de Productos Sanitarios de la Aemps, aseguró, en el marco del XXV Congreso Nacional de Derecho Sanitario, que la Agencia ya "está preparándose para solicitar la designación como organismo notificado bajo los reglamentos europeos y para que en pocos meses pueda dar el paso".




















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: