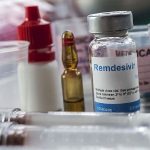
La Comisión Europea (CE) ha otorgado a Gilead una autorización condicional de comercialización para remdesivir que será comercializado bajo la denominación de Veklury, como tratamiento para la infección por SARS-CoV-2, el virus que causa covid-19.
Se trata de una decisión express que llega apenas ocho días después de la recomendación realizada por el Comité de Medicamentos de Uso Humano (CHMP), de la Agencia Europea de Medicamentos (EMA), frente a los tres meses que de forma habitual llega a durar la decisión de la CE.
Veklury está indicado para el tratamiento de COVID-19 en adultos y adolescentes (de 12 años de edad y mayores con un peso corporal de al menos 40 kg) con neumonía que requieren oxígeno suplementario.
“Agradecemos la rápida revisión de remdesivir por parte de la Agencia Europea del Medicamento, que reconoce la naturaleza sin precedentes de esta pandemia”, ha dicho Merdad Parsey, Chief Medical Officer de Gilead Sciences:. “Esta autorización de comercialización condicional es un importante paso adelante mientras seguimos trabajando juntos para responder a las necesidades de tratamiento de los pacientes en toda Europa”, concluyó Parsey.
Remdesivir ha sido estudiado en pacientes hospitalizados con COVID-19 con distintos grados de gravedad de la enfermedad. La autorización de comercialización condicional para remdesivir está respaldada por el ensayo global fase III llevado a cabo por el Instituto Nacional de Alergias y Enfermedades Infecciosas de EE. UU. (NIAID). Una autorización condicional de comercialización en Europa es inicialmente válida por un año, pero puede extenderse o convertirse en una autorización de comercialización incondicional, después de la presentación y evaluación de datos confirmatorios adicionales.
Los ensayos clínicos en curso continúan evaluando la seguridad y la eficacia de remdesivir, incluidos los estudios de remdesivir en combinación con medicamentos antiinflamatorios y en poblaciones especiales, que también incluyen pacientes pediátricos. Por otra parte, se están realizando investigaciones sobre nuevas formulaciones de remdesivir que pueden permitir su administración en etapas más tempranas de la enfermedad.




















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: