Las innovaciones terapéuticas que llegan hoy en día al mercado tienen unas características muy diferentes a las de hace solo unos años. Se trata de medicamentos “más complejos” de manejar y llegan con una “evidencia menos madura” al mercado, tal y como explicó Manuel Vazquez, Associate Principal Strategy de IQVIA en España durante el webinar ‘Acceso a nuevos medicamentos, un reto para el sistema sanitario’ organizado por la consultora.
El director general de IQVIA en España, José Luis Fernández, coincidió en señalar que “la innovación que viene es buena, pero tecnológicamente compleja” y que los sistemas sanitarios presentan “un estrés presupuestario muy relevante”. Por ese motivo, incidió en la necesidad de analizar todos los procesos y “trabajar de forma coordinada para incrementare el acceso”, aunque reconoció que “es más fácil decirlo, pero más difícil de conseguir”.
Fernández también puso el foco en que “el paciente debe estar ene l centro, pero esto no siempre ocurre” y que parte de la solución debe venir por la transparencia y disponibilidad de información en real world evidence (RWE), “que permita un sistema de provisión de salud basado en el valor”.
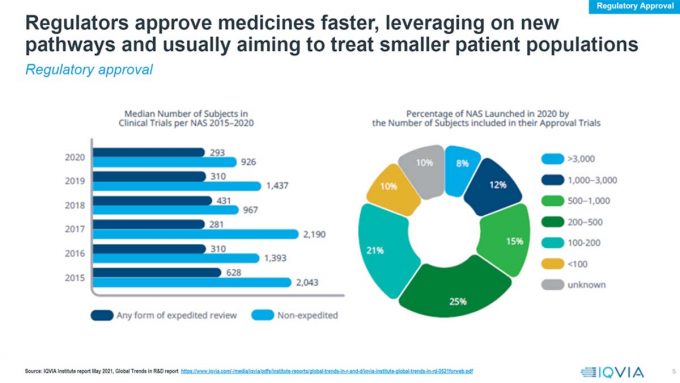
A lo largo del encuentro, Laia Aguilar, Principal Consulting and Services ha puesto de manifiesto que solo el 20% de los medicamnetos en desarrollo cuentan con más de 1.000 pacientes reclutados en ensayos clínicos. Por ese motivo, Daniel Callejo, Engagement Manager de IQVIA considera necesario “rediseñar los procesos de precio y financiación para adaptarlos a este tipo de innovación”.
Callejo ha puesto encima de la mesa otras cuestiones que serían necesarias para afrontar con éxito la entrada de la innovación en nuestro país. Entre otras ha mencionado la transparencia en los procesos, especialmente en los procedimientos intermedios de la financiación y fijación de precios.
Además, este experto, ha señalado la necesidad de repensar los modelos de referencia internacional de precios que provocan “retrasos” en el acceso, especialmente, en los países que tienen un pool más amplio de países referencia.
Por otro lado, también Callejo también aboga por implementar formas alternativas de financiación de las innovaciones, para lo que hace falta desarrollar sistemas de registro de la evidencia en vida real.
Desde el punto de vista de la industria también recomienda el diseño de estrategias anticipadas de distribución y partenariado entre compañías para incrementar el número de mercados a los que acceden y establecer estrategias que aseguren el lanzamiento con excelencia. En relación con el tipo de compañía, Callejo ha señalado que las grandes multinacionales lanzan sus productos en muchos más países que los pequeños y medianos laboratorios, algo que tiene mucha importancia dado que el 75% de los fármacos en desarrollo lo son, en la actualidad, por compañías pequeñas y medianas.
Este experto también cree necesario que se valoren las eficiencias y beneficios que los medicamentos “pueden tener sobre la sociedad y no solo como coste para el sistema de salud”.
Acceso a la innovación
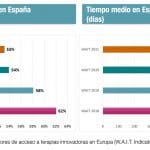
La consultora ha realizado un repaso sobre el acceso a la innovación en nuestro país y en Europa. Laia Aguilar, Principal Consulting and Services de IQVIA ha revisado los resultados del estudio WAIT que analiza el acceso a la innovación en los diferentes países europeos en los últimos años. De acuerdo con este estudio, de los 152 lanzamientos realizados entre 2016-2019, en Europa, solo 82 cuentan con precio y reembolso en España, cifra que estando por encima de la media de la UE, se encuentra lejos de los grandes países europeos.
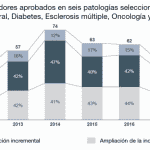
Por su parte, Manuel Vázquez ha explicado que en los últimos años “se ha visto un incremento significativo de lanzamiento de medicamentos innovadores”. En concreto, entre 2016-2020 ha habido un 26% de incremento respecto a los cinco años anteriores. En relación con la tipología, ha destacado el incremento que ha habido en medicamentos huérfanos, anticuerpos monoclonales y terapia celular y génica.
Vázquez ha explicado las dinámicas de lanzamientos de innovaciones que se producen en Europa y que condicionan el acceso en la mayoría de los países. El acceso se inicia en los países con precio libre de lanzamiento (Alemania, Suecia y Suiza), y posteriormente van avanzando los que tienen “cestas de referencias de precio” más pequeñas, como pueden ser Holanda, Austria, Italia o Francia. Los países con mayor retraso, entre los que se encuentra España, son los que tienen un mayor de países que se toman como referencia para los precios.
Este experto también ha destacado que en nuestro país existen importantes diferencias de plazos para el acceso según las distintas comunidades autónomas.





















 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: