El Instituto Nacional de Gestión Sanitaria (Ingesa) ha publicado en plenas navidades, concretamente el pasado 27 de diciembre, los pliegos de un acuerdo marco para la adquisición de medicamentos biosimilares.
Se trata de un acuerdo marco que viene a reintentarse después de que Ingesa tuviera que desistir del anterior, convocado a principios de 2020, ante las críticas tanto del sector como de las propias comunidades autónomas participantes.
La nueva edición podría seguir la misma senda ya que, como ha constatado Diariofarma, presenta importantes deficiencias que podrían suponer dificultades para finalmente llegue a su fin.
De acuerdo con fuentes de la industria, las deficiencias encontradas en los pliegos llegan a ser de tal calado que incluyen en la lista de comunidades autónomas adheridas al acuerdo marco a regiones que, como Aragón o Murcia, han publicado su propio acuerdo marco para la compra de algunos de los biosimilares que ahora Ingesa incluye en sus pliegos. De este modo, aunque en los pliegos se especifica que se han adherido diez comunidades autónomas (Aragón, Asturias, Baleares, Cantabria, Castilla y León, Extremadura, La Rioja, Madrid, Murcia, Navarra), además, del Ministerio de Defensa y el propio Ingesa para Ceuta y Melilla, la realidad es que al menos Aragón, Murcia y Baleares tienen en marcha su propia compra de biosimilares, por lo que sería “ilegal, ya que no se puede licitar dos veces el mismo bien”, según las fuentes de la industria.
A este respecto, cabe señalar que, en relación con los pliegos de 2020, Comunidad Valenciana y Galicia ya no participarán en la nueva edición de este acuerdo marco con Ingesa, aunque se suma Navarra para uno de los lotes. Por ese motivo, para estas fuentes de la industria, “no tiene sentido” la convocatoria de Ingesa, ya que muchas autonomías tienen en marcha su propio proceso de compra de biosimilares, están en camino del mismo o “no quieren obligarse a cambiar continuamente los tratamientos y dificultar la gestión a los servicios de farmacia para asegurar la continuidad de los tratamientos en pacientes estabilizados”.
Además, los pliegos tienen otra gran pega en relación con los criterios de adjudicación en los contratos derivados ya que se indica que se podrán valorar “condicionantes objetivos de índole clínica o logística”, pero no se especifica cuáles podrían ser. Esto hace “imposible” realizar una oferta ya que no es posible conocer si las mejoras clínicas que un medicamento o logísticas que una compañía puede ofrecer serán las que se valoren por una comunidad autónoma o, por el contrario, serán otras. “Así no se puede establecer un precio para las ofertas”, claman las fuentes de la industria.
Como balance, las personas de la industria consultada consideran que el nuevo pliego es un “copia-pega del anterior y lo que han cambiado, a peor”, por lo que no tiene “mucho sentido” haber realizado esta convocatoria. Además, señalan que la publicación de los pliegos ha cogido “con el pie cambiado” a algunas comunidades, que no esperaban este acuerdo marco.
Por todo ello, las fuentes de la industria vaticinan que los pliegos “están abocados al fracaso” ya que serán recurridos por diferentes compañías y serán “muy probablemente” anulados por los organismos competentes.
Diez lotes
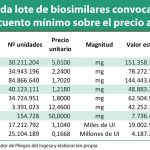
El nuevo acuerdo marco incorpora a sus pliegos un nuevo medicamento (bevacizumab) que se suma a los nueve anteriores (adalimumab, etanercept, infliximab, rituximab, trastuzumab, somatotropina, pegfilgrastim, epoetina alfa y filgrastim).
El nuevo concurso se convoca para dos años, con una posible prórroga por otro más y está valorado en un total de 370,76 millones de euros. Esta cifra supone una reducción del 33,6% respecto del anterior acuerdo marco que ascendía a más de 558 millones de euros.

























 Nicolas Gonzalez Casares:
Nicolas Gonzalez Casares: