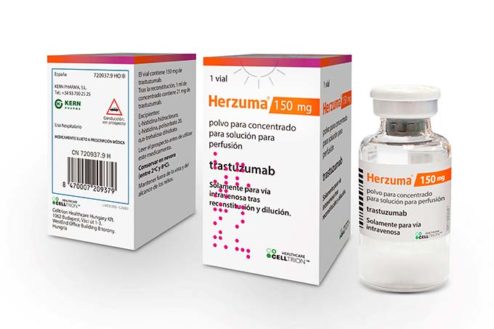
Kern Pharma Biologics ha lanzado en España y Portugal Herzuma, el biosimilar de trastuzumab desarrollado por Celltrion del que la firma española tiene los derechos de comercialziación para toda la península ibérica.
La firma de biosimilares de Kern Pharma pone a disposición de los clínicos tres anticuerpos monoclonales biosimilares (Remsima (infliximab), Truxima (rituximab) y Herzuma (trastuzumab), siendo la única compañía en nuestro país en hacerlo.
Además, con el lanzamiento de Herzuma, Kern Pharma vuelve a ser el laboratorio pionero en el lanzamiento de un biosimilar, como ya ocurrió con Remsima y Truxima.
Para el director general de Kern Pharma, Manuel Garrido, “este nuevo lanzamiento supone un paso crucial en la consolidación de nuestra división de biosimilares, Kern Pharma Biologics, y nos posiciona como un laboratorio de referencia en este ámbito. Fruto de nuestro compromiso con la innovación y del esfuerzo por poner al alcance de los profesionales y de los pacientes las últimas terapias disponibles, somos la única compañía española que comercializa tres anticuerpos monoclonales biosimilares en la península ibérica”.
La apuesta biológica de Kern
En 2015 la compañía con base en Terrasa lanzó su primer biosimilar de infliximab y dos años después el de rituximab. Desde entonces, la compañía ha seguido trabajando junto a Celltrion Healthcare, una de las principales biotecnológicas fabricantes de este tipo de fármacos y con mayor experiencia en este ámbito, en el lanzamiento de nuevos fármacos biosimilares.
Es de esperar que el acuerdo entre Kern y Celltrion se amplíe para los próximos desarrollos que tiene en marcha la compañía coreana, entre los que destacan bevacizumab (biosimilar de Avastin); etanercept (de Enbrel); cetuximab (de Erbitux); palivizumab (de Synagis) y adalimumab (de Humira).
Herzuma es un anticuerpo monoclonal humanizado aprobado por la Agencia Europea del Medicamento (EMA) para las mismas indicaciones terapéuticas que el fármaco biológico de referencia: cáncer de mama precoz, cáncer de mama metastásico y cáncer gástrico metastásico. Además, este fármaco, con el mismo mecanismo de acción que el fármaco biológico de referencia, “ha demostrado comparabilidad en términos de eficacia y seguridad”, explica Kern.














 César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:
César Hernández, director general de Cartera y Farmacia del Ministerio de Sanidad:  Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:
Kilian Sánchez, secretario de Sanidad del PSOE y portavoz de la Comisión de Sanidad del Senado.:  Rocío Hernández, consejera de Salud de Andalucía:
Rocío Hernández, consejera de Salud de Andalucía:  Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):
Nicolás González Casares, eurodiputado de Socialistas & Demócratas (S&D - PSOE):  Juan José Pedreño, consejero de Salud de Murcia:
Juan José Pedreño, consejero de Salud de Murcia: